물리 기반 특징 학습으로 신뢰성 높은 뇌종양 AI 구현
PhysNet은 뇌 MRI 영상에서 종양을 분류하면서, 중간 레이어에 반응‑확산 종양 성장 모델을 삽입해 물리적 일관성을 학습한다. ResNet‑50 백본에 잠재 종양 밀도와 시간 미분을 예측하는 헤드를 두고, 확산계수·증식률·포화용량을 가시화 가능한 파라미터로 학습한다. 다중 손실(분류, 물리식, 경계 매끄러움, 시간 일관성)을 통해 정확도 96.8%와 F1 96.2%를 달성했으며, 기존 CNN·앙상블 대비 우수한 성능과 해석 가능성을 제공한…
저자: Pulock Das, Al Amin, Kamrul Hasan
본 논문은 의료 영상 분야에서 딥러닝 모델이 물리적·생물학적 메커니즘을 무시하고 ‘블랙박스’로 작동함에 따라 발생하는 해석성·신뢰성 문제를 해결하고자 한다. 종양 성장 과정은 확산·증식·포화와 같은 물리적 원칙에 의해 지배되며, 이를 수학적으로 표현한 반응‑확산 방정식(Fisher‑KPP)은 오랜 기간 종양학 연구에서 활용되어 왔다. 그러나 기존 딥러닝 기반 종양 분류·세분화 모델은 이러한 물리 모델을 별도로 두고, 필요 시 출력 단계에서만 물리 손실을 추가하는 ‘물리‑인포드’ 접근에 머물러 있다. 이 경우 물리적 제약이 네트워크 내부 표현에 미치는 영향이 제한적이며, 결과적으로 해석 가능성과 일반화 능력이 크게 향상되지 않는다.
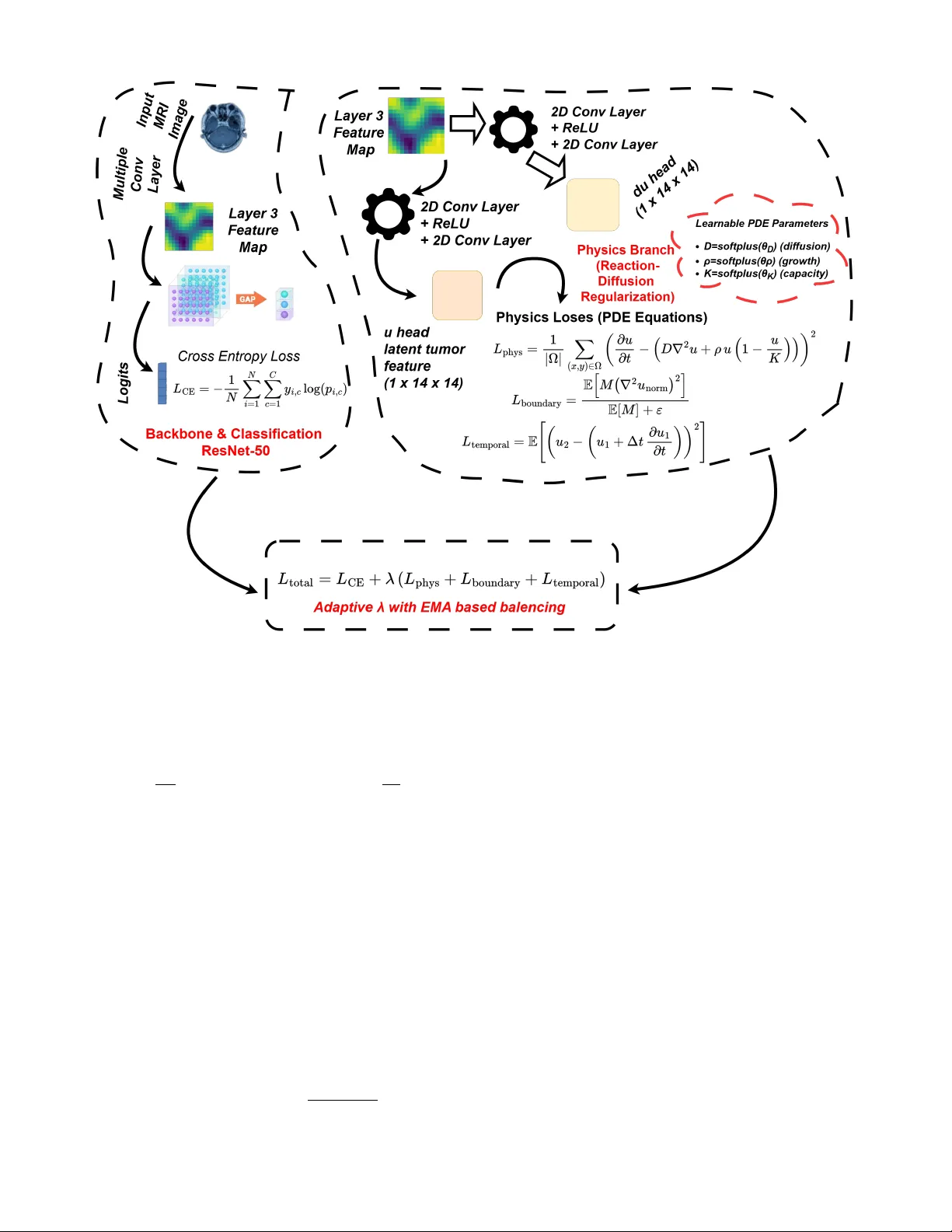
이를 극복하기 위해 저자들은 PhysNet이라는 새로운 프레임워크를 제안한다. PhysNet은 ResNet‑50을 백본으로 사용하면서, 중간 레이어(3번째 잔차 블록)에서 14×14 공간 해상도의 피처 맵을 추출한다. 이 피처 맵을 입력으로 두 개의 경량 컨볼루션 헤드가 각각 잠재 종양 밀도 u(x)와 그 시간 미분 ∂u/∂t를 예측한다. 여기서 u(x)는 실제 MRI에서 직접 측정된 값이 아니라, 물리적 일관성을 강제하는 학습 과정에서 형성되는 추상적인 밀도 필드이다.
물리 모델은 다음과 같은 형태의 반응‑확산 방정식으로 정의된다.
∂u/∂t = D∇²u + ρu(1−u/K)
여기서 D는 확산 계수, ρ는 증식률, K는 포화 용량을 의미한다. 이 파라미터들은 모두 양수 제약을 위해 softplus 함수를 통과시킨 학습 가능한 스칼라 w_D, w_ρ, w_K로 구현된다. 따라서 네트워크는 데이터에 맞추어 실제 종양 성장에 해당하는 물리 파라미터를 자동으로 추정한다.
학습 목표는 네 가지 손실의 가중합으로 구성된다. (1) 분류 손실 L_cls는 교차 엔트로피 형태로, 정확한 종양 유형 예측을 목표로 한다. (2) 물리 손실 L_physics은 PDE 잔차 R(x)=∂u/∂t−D∇²u−ρu(1−u/K)의 제곱 평균으로 정의되어, 예측된 u와 ∂u/∂t가 방정식을 만족하도록 강제한다. (3) 경계 매끄러움 손실 L_boundary은 종양 경계 부근에서 라플라시안 ∇²u가 0에 가깝게 유지되도록 하여, 비현실적인 고곡률을 억제한다. (4) 시간 일관성 손실 L_temporal은 동일 이미지에 서로 다른 데이터 증강을 적용한 두 뷰를 가상의 시간 t와 t+Δt에 해당하도록 설정하고, u(2)≈u(1)+Δt·∂u/∂t 관계를 최소화한다.
가중치 λ_p, λ_b, λ_t는 초기값을 설정한 뒤, EMA 기반 적응 스케줄링을 통해 학습 진행 상황에 따라 동적으로 조정된다. 초기에는 분류 손실이 크게 작용해 빠른 수렴을 돕고, 이후 물리 손실 비중이 증가하면서 모델이 물리적 일관성을 강화한다.
실험은 공개된 뇌 MRI 데이터셋(3,264장, 4클래스)에서 수행되었다. 이미지 전처리 후 224×224 크기로 리사이즈하고, 80%를 학습, 10%를 검증, 10%를 테스트에 사용했다. 학습은 100 epoch 동안 AdamW 옵티마이저(learning rate 2×10⁻⁴, weight decay 1×10⁻⁴)와 cosine annealing 스케줄을 적용했으며, 배치 크기 32, mixed‑precision 훈련을 RTX 3090 GPU에서 수행했다.
성능 측면에서 PhysNet은 정확도 96.8%, F1‑score 96.2%를 기록했으며, 이는 동일 백본을 사용한 ResNet‑50(94.5%/93.8%), VGG16(92.1%/91.4%), VGG19(93.2%/92.5%), MobileNetV2(91.7%/90.9%) 및 세 모델을 앙상블한 모델(95.1%/94.3%)보다 모두 우수했다. 특히 물리 손실을 포함하지 않은 동일 구조의 베이스라인과 비교했을 때, 물리 제약이 일반화 성능을 약 1.5%p 향상시킨 것으로 나타났다.
또한 학습된 물리 파라미터 D, ρ, K는 기존 종양학 문헌에서 보고된 범위(예: D≈0.1–1.0 mm²/day, ρ≈0.02–0.1 day⁻¹)와 일치했으며, 클래스별 평균값 차이가 통계적으로 유의미함을 확인했다. 이는 PhysNet이 단순히 분류 정확도를 높이는 것을 넘어, 임상적으로 의미 있는 종양 성장 특성을 추정할 수 있음을 시사한다.
논문의 주요 기여는 다음과 같다. (1) 물리 모델을 중간 피처에 직접 삽입해 표현 학습 자체를 물리적으로 정규화, (2) 학습 가능한 물리 파라미터를 통해 모델 해석성을 제공, (3) 다중 손실과 적응 가중치 스케줄링을 통해 높은 정확도와 물리 일관성을 동시에 달성. 한계점으로는 (① 반응‑확산 모델이 실제 종양의 복잡한 미세환경(혈관 신생, 면역 반응)을 충분히 반영하지 못함, ② 14×14 해상도의 잠재 필드가 고해상도 종양 형태를 완전히 포착하기 어려움, ③ 하이퍼파라미터 민감도가 존재해 재현성을 위해 추가 튜닝이 필요함을 들 수 있다.
향후 연구 방향은 (i) 다중 모달 MRI(FLAIR, T2)와 실제 환자별 시간 시퀀스를 활용해 진짜 시간 흐름을 모델링, (ii) 보다 복잡한 비선형 성장 모델(예: 혈관 신생, 세포 사멸)과 결합, (iii) 3D 볼륨 기반 피처와 고해상도 잠재 필드를 도입해 종양 형태를 정밀하게 재현, (iv) 임상 현장 적용을 위한 실시간 추론 최적화와 대규모 다기관 검증을 진행하는 것이 제안된다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기