대장암 원격 전이 예측을 위한 디지털 조직 표현형 서명
본 연구는 전자현미경 이미지에서 자동화된 세포 유형 및 이웃 관계를 분석해 6가지 조직 표현형을 도출하고, 이들 중 평활근 비율과 염증 비율이 원격 전이와 무전이 생존에 독립적인 예측인자로 작용함을 보여준다.
저자: Korsuk Sirinukunwattana, David Snead, David Epstein
**배경 및 목적**
대장암에서 원격 전이는 사망의 주요 원인이며, 조기 위험 예측이 치료 전략 수립에 핵심이다. 기존 연구는 종양 세포 자체뿐 아니라 종양 미세환경(스트로마, 면역세포, 괴사 등)의 역할을 강조했지만, 이를 정량적으로 평가하는 방법은 아직 제한적이었다. 본 연구는 디지털 병리 이미지에서 자동화된 세포 유형 및 이웃 관계 분석을 통해 새로운 조직 표현형 서명을 도출하고, 이 서명이 원격 전이와 무전이 생존에 미치는 영향을 평가한다.
**자료 및 방법**
- **대상**: 영국 University Hospitals Coventry and Warwickshire (UHCW, n=78)와 카타르 Hamad General Hospital (HGH, n=30)에서 수집된 T3/T4, N0, M0/M1 단계의 대장암 환자 108명.
- **이미지**: H&E‑염색 슬라이드를 Whole‑Slide Image(WSI) 형태로 스캔.
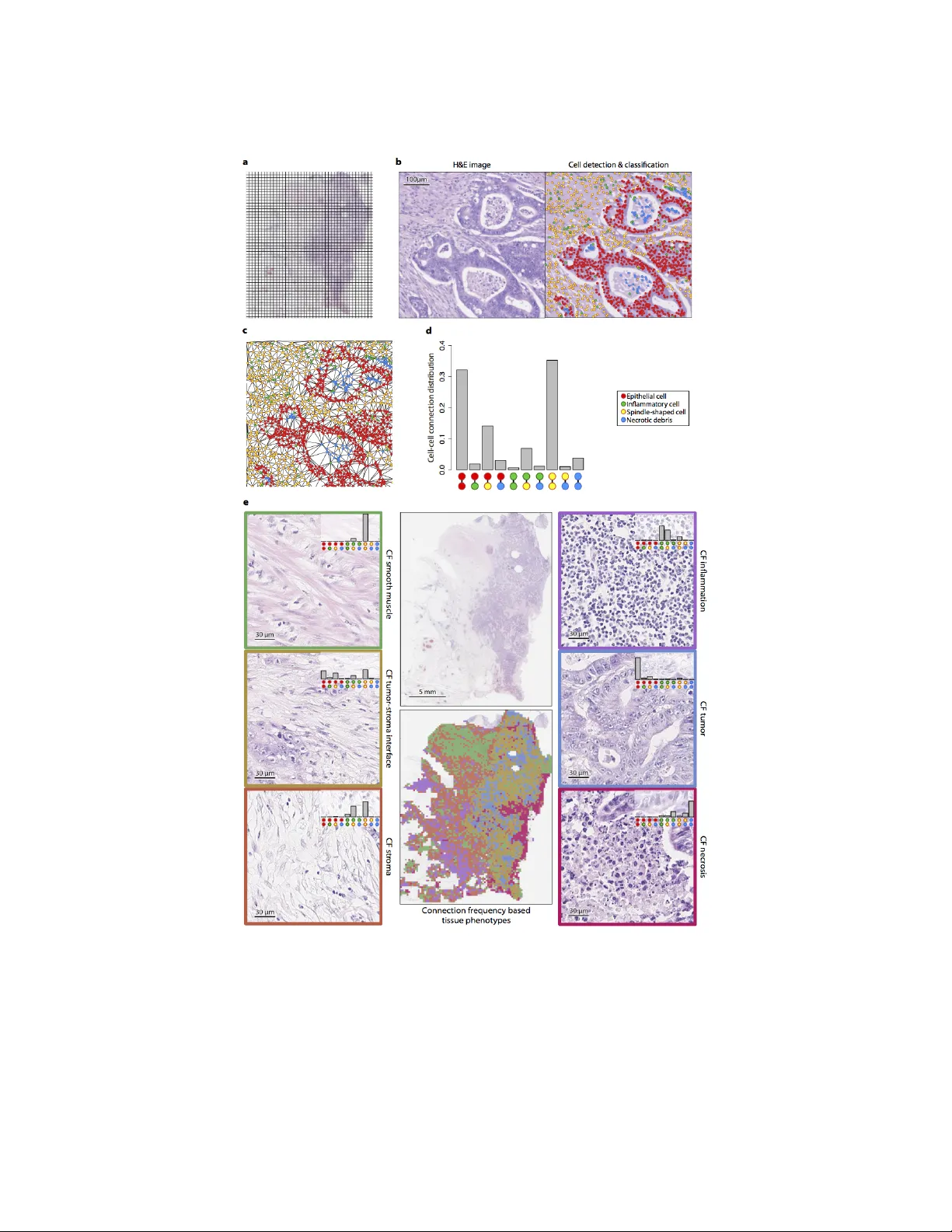
- **세포 분류**: 저자들이 이전에 개발한 AI 모델(딥러닝 기반)로 네 종류의 세포(악성 상피, 방추형, 염증, 괴사)를 형태학적 특징과 주변 조직 맥락을 이용해 자동 식별.
- **패치 단위 분석**: WSI를 작은 정사각형 서브이미지(패치)로 분할하고, 각 패치 내에서 세포‑세포 인접 관계를 그래프(노드=세포, 엣지=인접)로 모델링.
- **조직 표현형 도출**: 인접 빈도(CF)를 특징 벡터로 변환한 뒤, 비지도 군집화(예: k‑means)로 6가지 CF 기반 조직 표현형을 정의: 평활근, 염증, 종양‑스트로마 경계, 종양, 스트로마, 괴사.
- **색상·텍스처 기반(AP) 세그멘테이션**: 전통적인 이미지 분석으로 8가지 조직 유형(종양, 스트로마, 연부 조직, 점막, 평활근, 괴사, 지방, 염증)을 자동 분할하고, CF와 AP 간 상관관계(Spearman ρ=0.43–0.70)를 평가.
- **통계 분석**:
- **연관성 검증**: CF 표현형 비율과 임상 변수(T‑stage, 분화도 등) 간 Mann‑Whitney U 테스트.
- **로지스틱 회귀**: 원격 전이 발생 여부를 종속 변수로, 각 CF/ AP 비율을 독립 변수로 단변량·다변량 분석.
- **Cox 비례위험 모델**: 무전이 생존(DMFS)과 각 지표 간 관계를 평가, Kaplan‑Meier 생존곡선 및 로그‑랭크 검정 수행.
**주요 결과**
1. **CF 평활근 비율**은 원격 전이 위험을 약 2.3배 증가시키는 독립적인 위험인자이며, 다변량 로지스틱 회귀에서도 p<0.05.
2. **CF 염증 비율**은 전이 위험을 약 0.3배 감소시키는 보호인자로 작용한다.
3. **AP 염증 비율**은 단변량에서만 유의미(p≈0.027)하고, 다변량에서는 경계 수준(p≈0.056)이다.
4. **Cox 분석**에서 CF 평활근 비율이 높은 경우 위험비(HR)≈2.5(다변량)로 DMFS를 크게 악화시킨다. 반면, CF 염증 비율과 AP 염증 비율은 위험을 각각 0.4배 정도 감소시킨다.
5. CF 평활근과 염증 비율 사이에 강한 음의 상관관계(ρ≈‑0.65)가 존재해, 두 변수를 동시에 모델에 포함하면 다중공선성 문제가 발생한다.
6. CF 스트로마 비율도 단변량에서 유의미(p≈0.032)했으나, 다변량에서는 독립성을 확인하지 못했다.
**논의**
- **임상적 의의**: 전통적인 병리학적 평가와 달리, 전체 슬라이드에 걸친 자동화된 정량적 지표는 관찰자 간 변이를 최소화하고, 미세환경의 복합적 상호작용을 포착한다. 특히 평활근 비율은 종양 주변 근육층의 구조적 변화를 반영할 가능성이 있으며, 이는 종양 침습 및 전이와 연관될 수 있다.
- **방법론적 강점**: 전체 슬라이드 분석, 4가지 세포 유형을 동시에 고려한 네트워크 기반 접근, 비지도 군집화를 통한 해석 가능한 조직 표현형 도출.
- **제한점**: 코호트 규모가 작고, 외부 검증이 부족하며, AI 모델이 세포 아형(예: CD8⁺ T세포 vs. 조절 T세포)을 구분하지 못한다. 또한, 평활근과 염증 비율 간 상관관계로 인해 실제 임상 적용 시 어느 하나를 선택해야 하는지에 대한 가이드라인이 필요하다.
**향후 연구 방향**
다기관·다국가 대규모 코호트와 전이성 조직, 유전체·전사체 데이터와의 통합을 통해 모델의 일반화와 생물학적 메커니즘 규명을 확대해야 한다. 또한, 실시간 병리 워크플로우에 통합할 수 있는 소프트웨어 플랫폼 개발과, 병리학자와 임상의가 해석 가능한 시각화 도구 제공이 필요하다.
**결론**
본 연구는 디지털 병리 이미지를 활용한 자동화된 조직 표현형 서명이 대장암 원격 전이 위험 및 무전이 생존을 예측하는 독립적인 바이오마커가 될 수 있음을 입증하였다. 특히 CF 평활근 비율과 CF 염증 비율은 임상 의사결정에 활용될 잠재력을 지니며, 향후 정밀 의학 및 맞춤형 치료 전략 수립에 기여할 것으로 기대된다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기