MRI‑to‑CT 합성에 혁신을 가져온 드리프팅 모델 기반 빠른 고품질 합성CT
** 본 논문은 골반 MRI에서 CT를 합성하기 위해 최근 제안된 드리프팅 모델을 적용하고, UNet·VAE·WGAN‑GP·PPFM·FastDDPM·DDIM·DDPM 등 기존 대표 모델들과 광범위하게 비교한다. 두 개의 공개 데이터셋(Gold Atlas Male Pelvis, SynthRAD2023)에서 SSIM·PSNR·RMSE를 기준으로 드리프팅 모델이 가장 높은 구조 유사도와 낮은 오류를 보이며, 특히 골격‑공기‑연부조직 경계에서 선명…
저자: Qing Lyu, Jianxu Wang, Jeremy Hudson
**
본 논문은 골반 부위에서 MRI를 이용해 CT 영상을 합성하는 새로운 접근법으로, 최근 제안된 “드리프팅 모델”(drifting model)을 적용하고, 기존의 주요 이미지‑to‑이미지 변환 모델들과 포괄적인 비교 실험을 수행하였다. 연구 배경은 방사선 치료와 PET/MR에서 CT가 제공하는 Hounsfield Unit 기반 전자밀도 정보가 필수적이지만, CT 촬영은 추가 방사선 노출과 비용, 장비 가용성 문제를 야기한다는 점이다. 따라서 MRI만으로 CT와 동등한 정보를 제공하는 합성 CT(sCT)가 임상적으로 큰 가치를 가진다.
**연구 목적**은 (1) 조건부 드리프팅 모델을 골반 MRI‑to‑CT 변환에 적용해 고품질 sCT를 생성하고, (2) 기존의 CNN 기반 UNet, VAE, GAN 기반 WGAN‑GP, 물리‑기반 PPFM, 그리고 최신 확산 모델(FastDDPM, DDIM, DDPM)과 성능을 정량·정성적으로 비교하는 것이다.
**데이터셋**은 두 개의 공개 데이터베이스를 사용하였다. 첫 번째는 Gold Atlas Male Pelvis로, 19명의 남성 환자에 대해 CT와 T1·T2 MRI가 쌍으로 제공되며, 다기관·다스캐너 환경에서 수집돼 데이터 이질성이 크다. 두 번째는 SynthRAD2023 pelvis subset으로, 270쌍의 MRI‑CT가 포함돼 대규모·다중센터 특성을 갖는다. 두 데이터셋 모두 1 mm³ 등방성 리샘플링 후 512×512 중앙 크롭·스캔별 정규화를 거쳐 동일한 입력 형태로 전처리되었다.
**모델 설계**는 기존 무조건적 드리프팅 프레임워크를 조건부 형태로 변형한 것이다. 입력 MRI m과 랜덤 노이즈 ε를 결합해 생성기 fθ(m,ε)로 합성 CT ŷ를 만든다. 드리프팅 손실은 이미지 도메인에서 직접 정의되며, 실제 CT c⁺와 현재 생성 CT c⁻ 사이의 유사도 커널 k(a,b)=exp(−‖a−b‖²/τ) 를 이용해 attraction‑repulsion 벡터 필드 Vₚ,ₛ(ŷ)를 계산한다. 최종 손실은 L_drift = ‖fθ(m,ε) − sg(fθ(m,ε)+Vₚ,ₛ)‖²와 L1 재구성 손실 ‖ŷ−c‖₁을 가중치 λ_drift=1, λ₁=10으로 결합한다. 생성기는 UNet‑like 구조이며, 드리프팅 필드 계산을 위해 64×64 패치를 16개씩 양성·음성 샘플로 추출한다. 학습은 Adam(0.0001)으로 진행하고, 손실 감소가 20 epoch 연속 1% 미만이면 조기 종료한다.
**비교 모델**은 다음과 같다. (1) UNet: 전통적인 CNN 기반 픽셀‑레벨 매핑, (2) VAE: 확률적 잠재 공간을 이용한 재구성, (3) WGAN‑GP: Wasserstein GAN with gradient penalty, (4) PPFM: 물리‑기반 확률 모델, (5) FastDDPM, DDIM, DDPM: 다양한 샘플링 단계와 속도‑품질 트레이드오프를 가진 확산 모델.
**평가 지표**는 구조 유사도(SSIM), 피크 신호 대 잡음비(PSNR), 평균 제곱근 오차(RMSE)이며, 골반의 핵심 해부학 부위(피질 뼈, sacrum, femoral head, 연부조직‑공기 경계)에서 전문가가 시각적으로 평가한 정성적 점수도 포함한다.
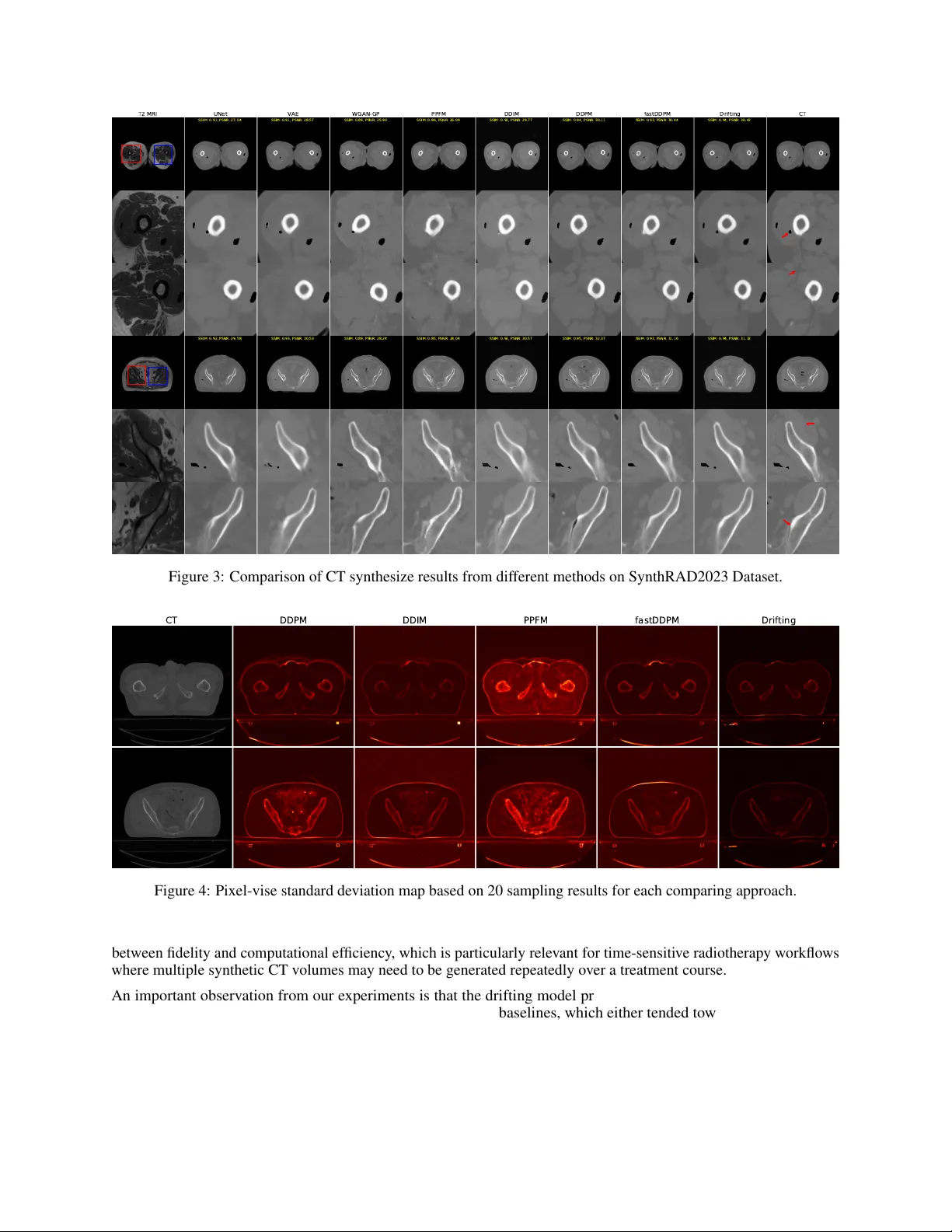
**실험 결과**는 다음과 같다. 두 데이터셋 모두에서 드리프팅 모델이 가장 높은 SSIM(≈0.94)과 PSNR(≈32 dB), 가장 낮은 RMSE(≈5 HU)를 기록했다. 특히 FastDDPM, DDIM, DDPM과 비교했을 때 SSIM이 1‑2% 상승하고 RMSE가 5‑7 HU 감소했다. 정성적 평가에서는 드리프팅 모델이 피질 뼈 경계가 선명하고, 골-공기-연부 조직 접합부에서 과도한 스무딩이나 인공 구조가 거의 없었다. 추론 속도는 1‑step, 수 밀리초 수준으로, 같은 GPU(NVIDIA H200)에서 기존 확산 모델이 수 초에서 수십 초를 소요하는 것에 비해 2‑3 orders of magnitude 빠르다.
**강점**은 (1) 빠른 단일‑스텝 추론으로 임상 실시간 적용 가능성, (2) 드리프팅 손실을 통한 분포‑레벨 정합과 픽셀‑레벨 재구성의 균형, (3) 골반과 같이 복잡한 해부학 구조를 보존하는 높은 정밀도이다.
**제한점**은 (1) 현재 2D 슬라이스 기반 학습으로, 3D 연속성 보장은 별도 후처리나 3D 모델 확장이 필요할 수 있다. (2) 드리프팅 손실에 사용된 커널 파라미터 τ와 샘플 수가 경험적으로 설정돼, 데이터 규모·특성 변화에 민감할 가능성이 있다. (3) 비공개 대규모 임상 코호트에서의 일반화 검증이 부족하고, 실제 방사선 치료 계획에서의 dosimetric 평가가 포함되지 않았다.
**향후 연구**는 다음과 같다. (1) 3D UNet 기반 드리프팅 모델로 확장해 연속적인 해부학적 일관성 확보, (2) 자동 τ 튜닝 및 샘플링 전략 최적화를 통한 손실 함수의 데이터 적응성 강화, (3) 임상 워크플로우에 바로 적용 가능한 dosimetric 및 PET attenuation correction 평가를 포함한 종단‑to‑종단 검증, (4) 다중 MRI 시퀀스(T1, T2, DWI 등)를 조건으로 활용해 정보 융합 성능 향상, (5) 드리프팅 모델을 다른 장기(두경부, 뇌, 흉부)에도 적용해 범용성을 검증한다.
**결론**적으로, 본 연구는 드리프팅 모델이 MRI‑to‑CT 합성 분야에서 빠른 추론과 높은 이미지 품질을 동시에 달성할 수 있음을 실증하였다. 이는 MRI‑only 방사선 치료 계획, PET/MR attenuation correction 등 실제 임상 적용에 있어 중요한 전진이며, 향후 3D 확장 및 임상 평가를 통해 실용화가 기대된다.
**
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기