CAPSUL 인간 단백질 서브셀룰러 위치 예측을 위한 3D 구조 기반 벤치마크
CAPSUL은 AlphaFold2 예측 구조와 UniProt·Human Protein Atlas의 실험적 라벨을 결합해 20 개의 세부 세포 구획으로 구분된 20 181개의 인간 단백질 데이터를 제공한다. 3Di 토큰과 Cα 좌표를 포함한 구조 정보와 고품질 라벨을 이용해 최신 시퀀스·구조 기반 모델을 평가했으며, 구조 입력이 서브셀룰러 위치 예측에 큰 이점을 주는 것을 입증했다. 또한 어텐션 메커니즘을 활용해 골지체 내 α‑헬릭스 패턴이 결정…
저자: Yicheng Hu, Xinyu Lin, Shulin Li
본 논문은 단백질 서브셀룰러 로컬라이제이션 예측에 구조 정보를 정식으로 도입한 최초의 대규모 벤치마크 “CAPSUL”(Comprehensive Human Protein Benchmark for Subcellular Localization)을 제안한다. 서론에서는 단백질 위치가 기능과 약물 표적 선정에 핵심적임을 강조하고, 기존 DeepLoc·setHARD와 같은 데이터셋이 구조 정보를 제공하지 않아 구조 기반 모델의 평가가 불가능함을 지적한다. 또한, 서열만으로는 노출되는 구조적 신호(예: 핵심 신호 서열, 조건부 노출 구조)를 포착하기 어렵다는 생물학적 근거를 제시한다.
관련 연구 파트에서는 시퀀스 기반 언어 모델(Transformer, CNN, LSTM)과 최근의 구조 기반 모델(GCN, Graphormer, 3Di 토큰 기반 트랜스포머)의 발전을 정리하고, 이들 모델이 단백질 설계·예측·생성 등에 성공했음에도 불구하고 서브셀룰러 로컬라이제이션 데이터가 부족해 적용이 제한돼 왔음을 설명한다.
데이터셋 구축 파트는 4단계 프로세스로 구성된다. 1) AlphaFold2에서 인간 단백질 20 504개를 다운로드하고, UniProt 활성 단백질만 남겨 20 401개로 축소한다. 2) 파편화된 구조 예측을 제외해 20 181개의 고품질 구조를 확보한다. 3) 각 단백질에 대해 Cα 좌표를 추출하고, FoldSeek을 이용해 3Di 구조 토큰을 생성한다. 4) UniProt과 Human Protein Atlas(HPA)에서 서브셀룰러 로컬라이제이션 어노테이션을 수집하고, 증거 코드(ECO)를 기반으로 라벨 신뢰도를 0·1·2로 구분한다. 라벨은 기존 DeepLoc의 10구획을 세분화해 20개의 세부 구획(핵, 핵막, 핵소체, 골지체, 미토콘드리아 등)으로 정의했으며, 전문가 검증을 거쳐 최종 통합하였다.
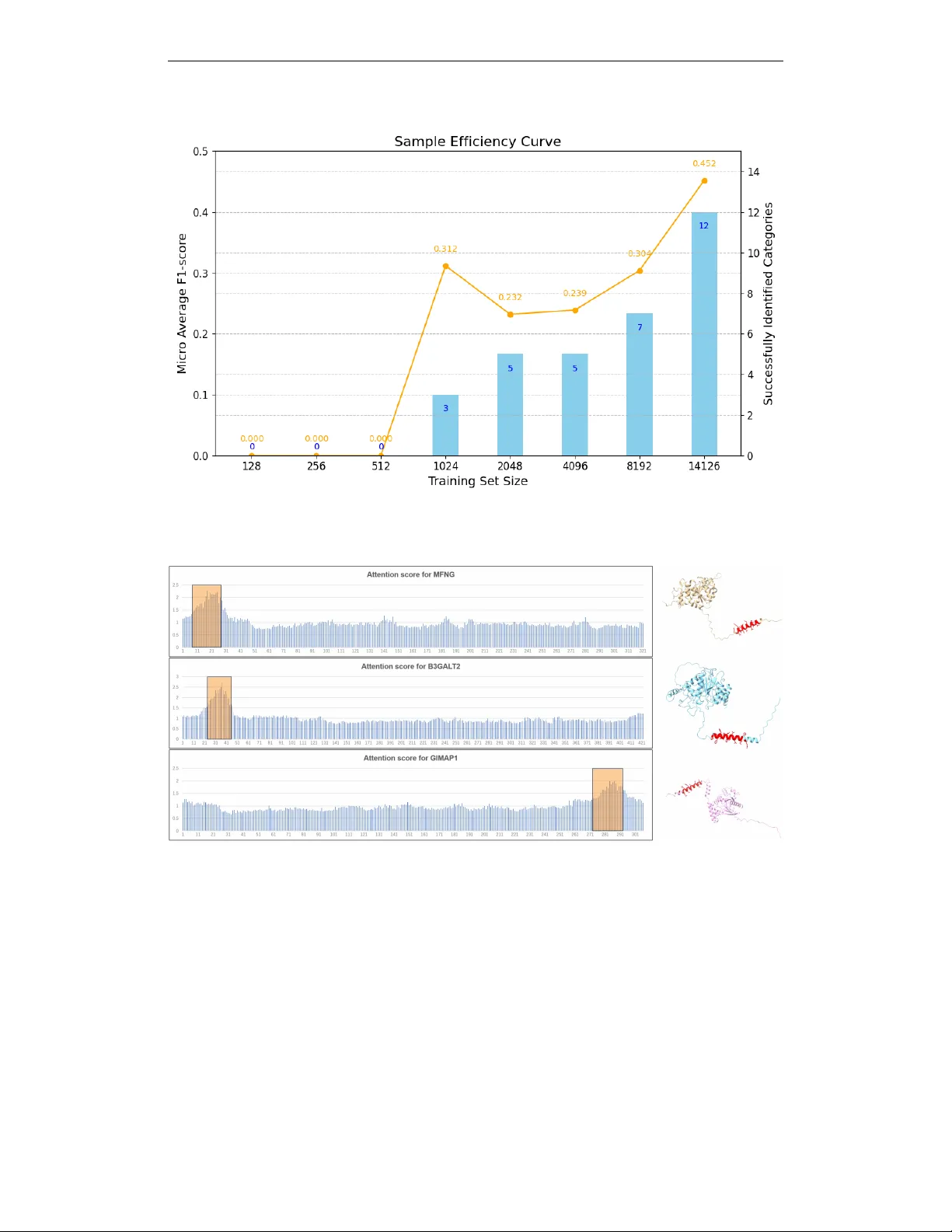
통계표(표 2)에서는 평균 2.51개의 라벨이 단백질당 부여되며, 최대 14개의 라벨을 갖는 경우도 있음을 보여준다. 전체 라벨 중 85.7%가 실험적 근거를 가지고 있어 데이터 신뢰도가 높다. 데이터는 70 %/15 %/15 % 비율로 학습·검증·테스트 셋으로 무작위 분할한다.
실험 파트에서는 최신 시퀀스 기반 모델(Evoformer, ProtBERT)과 구조 기반 모델(GCN, Graphormer, 3Di‑Transformer)을 CAPSUL에 적용해 성능을 비교한다. 구조 입력을 포함한 모델은 평균 F1‑macro 점수에서 4~7%p 상승했으며, 특히 골지체·핵막·미토콘드리아와 같이 구조적 특징이 뚜렷한 구획에서 큰 개선을 보였다. 라벨 불균형을 완화하기 위한 재가중치(reweighting)와 멀티라벨을 싱글라벨로 변환하는 전략도 각각 1~2%p의 추가 향상을 가져왔다.
해석 가능성 연구에서는 구조 기반 모델에 어텐션 메커니즘을 삽입해 각 잔기의 중요도를 시각화했다. 골지체 예측 사례에서 α‑헬릭스 영역이 높은 어텐션 가중치를 받아, 해당 2차 구조가 골지체 타깃팅 신호와 강하게 연관됨을 확인했다. 이는 기존에 알려진 서열 기반 신호와는 다른 구조 기반 패턴을 제시하며, AI 모델이 새로운 생물학적 인사이트를 제공할 가능성을 보여준다.
논문의 주요 기여는 다음과 같다. (1) 인간 단백질 20 181개에 대해 3D 구조(Cα 좌표·3Di 토큰)와 실험적 근거를 갖는 20개의 세부 서브셀룰러 라벨을 제공하는 최초의 데이터셋 구축, (2) 구조 기반 모델이 서브셀룰러 로컬라이제이션에 미치는 긍정적 영향을 실증, (3) 어텐션 기반 해석을 통해 구조적 패턴을 시각화하고 생물학적 의미를 도출.
마지막으로 한계점과 향후 연구 방향을 논의한다. AlphaFold2 예측 구조의 정확도 한계, 다중 라벨 간 상관관계를 충분히 모델링하지 못한 점, 그리고 현재 3Di 토큰이 백본 구조에 초점을 맞추어 side‑chain 정보를 충분히 반영하지 못한다는 점을 지적한다. 향후 실제 실험 구조와의 교차 검증, 라벨 상호작용을 고려한 멀티태스크 학습, 보다 풍부한 토큰화(예: side‑chain orientation, solvent accessibility) 등을 통해 데이터와 모델을 확장할 필요가 있다.
결론적으로 CAPSUL은 서브셀룰러 로컬라이제이션 분야에 구조 기반 딥러닝 연구를 본격화할 수 있는 토대를 제공하며, 향후 세포 생물학적 발견과 신약 개발에 중요한 역할을 할 것으로 기대된다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기