MRD를 진행무진행생존(PFS) 대리지표로 활용 가능성 메타분석
본 논문은 최소잔류질환(MRD)이 진행무진행생존(PFS) 및 전체생존(OS)과의 대리지표(surrogate) 역할을 할 수 있는지를 다중암종, 특히 여포성 림프종(FL)을 중심으로 메타분석하였다. 개인 수준과 시험 수준의 상관관계를 Buyse 등(2000) 프레임워크와 플라켓 코퓰라 모델을 이용해 평가했으며, 현재 FDA가 제시한 R² 기준(≥0.8)와 비교하였다. 결과는 FL에서 MRD와 PFS 간 개인 수준의 강한 연관성은 확인되었지만, 시…
저자: Jane She, Xiaofei Chen, Malini Iyengar
본 논문은 최소잔류질환(MRD)이 진행무진행생존(PFS) 및 전체생존(OS)과 같은 전통적인 임상시험 종말점(endpoint)의 대리지표(surrogate)로 활용될 수 있는지를 평가하기 위해 다중암종, 특히 여포성 림프종(FL)을 중심으로 메타분석을 수행하였다. 1992년 FDA가 도입한 가속 승인(Accelerated Approval) 경로는 조기 측정 가능한 대리지표를 기반으로 신약 승인을 가능하게 하며, MRD는 혈액암에서 매우 민감하게 잔류 암세포를 탐지할 수 있는 기술로 주목받고 있다.
연구진은 AstraZeneca 내부 정보실무팀이 2024년 2월부터 8월까지 PubMed, Embase, ClinicalTrials.gov, Trialtrove 등에서 “MRD”, “PFS”, “OS” 등 키워드로 검색한 결과를 바탕으로 두 팔(Randomized) 임상시험을 우선 선정하였다. 두 팔 연구가 충분히 확보되지 않은 경우에는 단일군 연구를 활용해 개인 수준 상관관계를 추정했으며, 이는 치료 효과를 반영하지 못한다는 제한점을 명시하였다. 최종적으로 FL에서는 7개의 논문 중 4개의 1차 치료(1L) 무작위 시험을 포함했으며, 각각 GALLIUM, RELEVANCE, UK NCRI, FOLL12 시험이다.
데이터 추출은 “ScanIt”이라는 픽셀 기반 소프트웨어와 R 패키지 “IPDfromKM”을 이용해 Kaplan‑Meier 곡선에서 개별 환자 데이터를 재구성하였다. 재구성된 IPD는 Cox 비례위험모형을 통해 PFS 위험비를, 로지스틱 회귀를 통해 MRD 음성률의 오즈비를 산출하는 데 사용되었다. 또한, 각 시험에서 MRD는 PCR 기반으로 최소 10⁻⁴ 민감도를 갖추었으며, 측정 시점은 유도 종료(EOI)에서 치료 종료까지 4~12개월 사이로 다양했다.
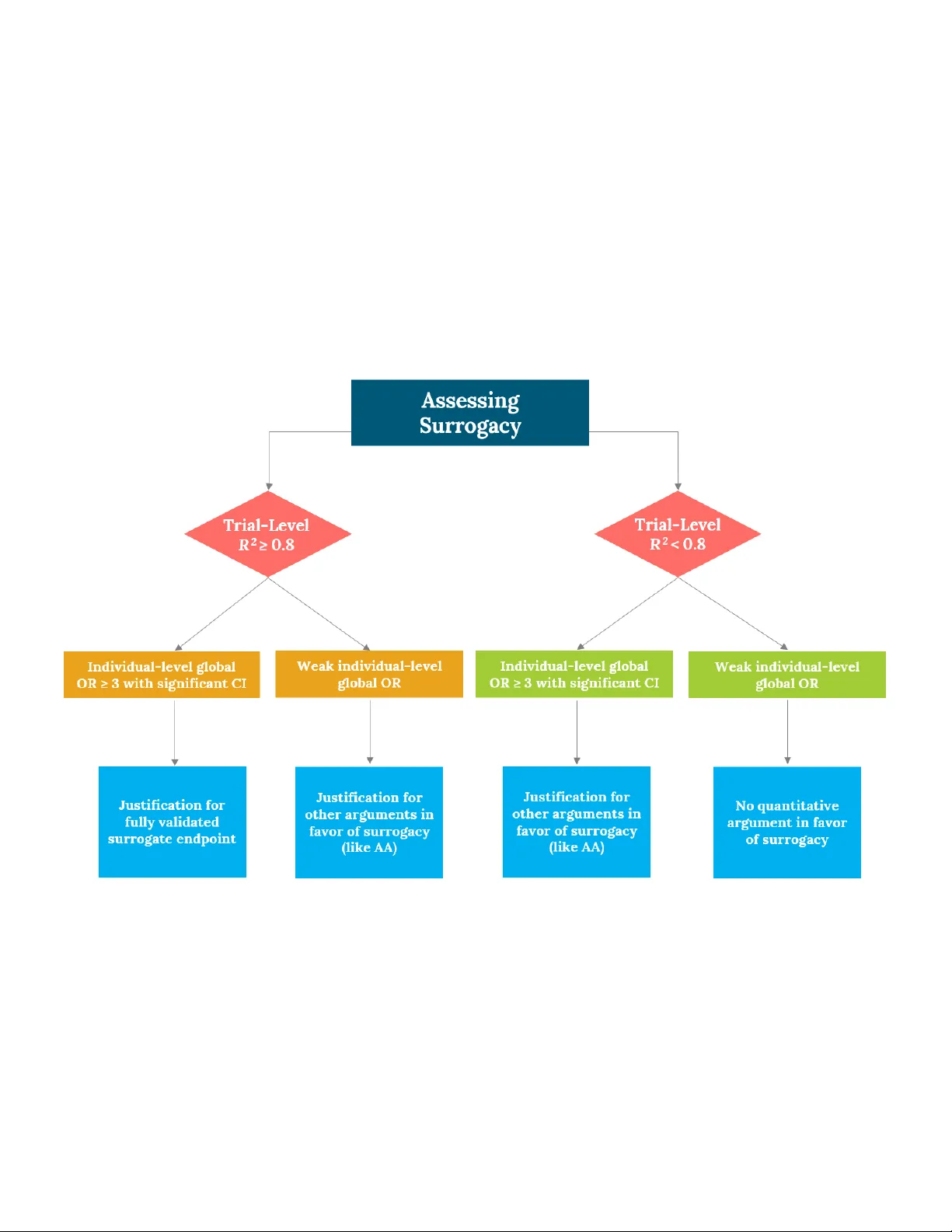
Surrogacy 평가는 Buyse et al.(2000)의 프레임워크를 채택했으며, 개인 수준과 시험 수준 두 차원에서 상관관계를 동시에 검토하였다. 시험 수준 상관관계는 세 가지 모델로 추정되었다. 첫 번째와 두 번째는 가중 최소제곱법(WLS)으로, 로그 위험비와 로그 오즈비를 각각 역분산 가중치와 표본 크기 가중치로 사용하였다. 세 번째는 이중변량 플라켓 코퓰라(bivariate Plackett copula) 모델로, 치료 효과 추정치의 불확실성을 반영하고 환자 수준 상관관계까지 동시에 고려한다. 플라켓 코퓰라 모델은 “global odds ratio”라는 지표를 제공하는데, 이는 MRD 음성 환자가 PFS 무진행 상태를 유지할 확률이 MRD 양성 환자에 비해 얼마나 높은지를 직관적으로 나타낸다.
분석 결과, 개인 수준에서는 플라켓 코퓰라 모델이 제공한 global odds ratio가 1.8~2.1 수준으로, MRD 음성인 환자가 PFS 사건을 겪을 위험이 현저히 낮음을 보여주었다. 이는 MRD가 강력한 예후인자임을 시사한다. 그러나 시험 수준에서는 R²_WLS가 0.247(95% CI 0–1)로 낮았으며, R²_Copula는 0.12(95% CI 0–0.64)로 하한이 0을 포함한다. FDA가 제시한 ‘강한 대리지표’ 기준인 R²≥0.8 및 하한 0.6을 충족하지 못한다는 점에서, 현재 데이터만으로는 MRD를 PFS의 공식적인 대리지표로 인정하기 어렵다.
연구는 또한 MRD 측정 방법과 시점의 이질성이 결과에 미치는 영향을 논의한다. FL 연구들에서 MRD는 모두 PCR 기반이었지만, 측정 시점이 유도 종료(EOI)와 치료 종료 사이에 차이가 있었으며, 이는 MRD와 PFS 사이의 상관관계에 변동성을 야기한다. 또한, 평균 추적 기간이 약 3.8~4년으로, 장기 OS와 비교했을 때 PFS와의 연관성을 충분히 평가하기엔 제한적일 수 있다.
통계적 한계로는 소규모 메타분석으로 인한 부트스트랩 신뢰구간의 폭이 넓고, 플라켓 코퓰라 모델의 2단계 추정에서 상관계수 신뢰구간이 음·양을 모두 포함할 경우 R² 값이 비논리적인 형태(하한 > 상한)로 나타날 수 있다는 점을 지적한다. 이는 표본수가 제한적인 상황에서 흔히 발생하는 문제이며, 결과 해석 시 주의가 필요하다.
결론적으로, MRD는 개인 수준에서 강력한 예후인자를 제공하지만, 현재 증거만으로는 시험 수준에서 PFS를 대체할 충분한 근거가 부족하다. 따라서 MRD를 가속 승인에서 ‘중간’ 지표로 활용해 조기 신약 접근성을 높이는 전략은 타당하지만, 정식 대리지표로 인정받기 위해서는 더 많은 무작위 대조군 연구와 표준화된 MRD 측정 프로토콜이 필요하다. 향후 연구에서는 다양한 혈액암 유형에 대한 대규모 메타분석, MRD 측정 시점 및 민감도 표준화, 그리고 장기 OS와의 연계 분석이 요구된다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기