의료 영상 분류를 위한 GLoG 바이필터링
본 논문은 Gaussian‑Laplacian of Gaussian(G‑LoG) 연산을 이용해 의료 영상에 대한 이중 파라미터 필터링을 정의하고, 이를 다중 파라미터 영속 동형학 모듈에 적용한다. bounded function 형태로 모델링한 volumetric 이미지에 대해 최대 노름에 대한 안정성을 증명했으며, MedMNIST 데이터셋 실험에서 단일 파라미터 필터링 및 최신 딥러닝 베이스라인을 능가함을 보였다. 특히, 위상 특징만을 사용한 간…
저자: Qingsong Wang, Jiaxing He, Bingzhe Hou
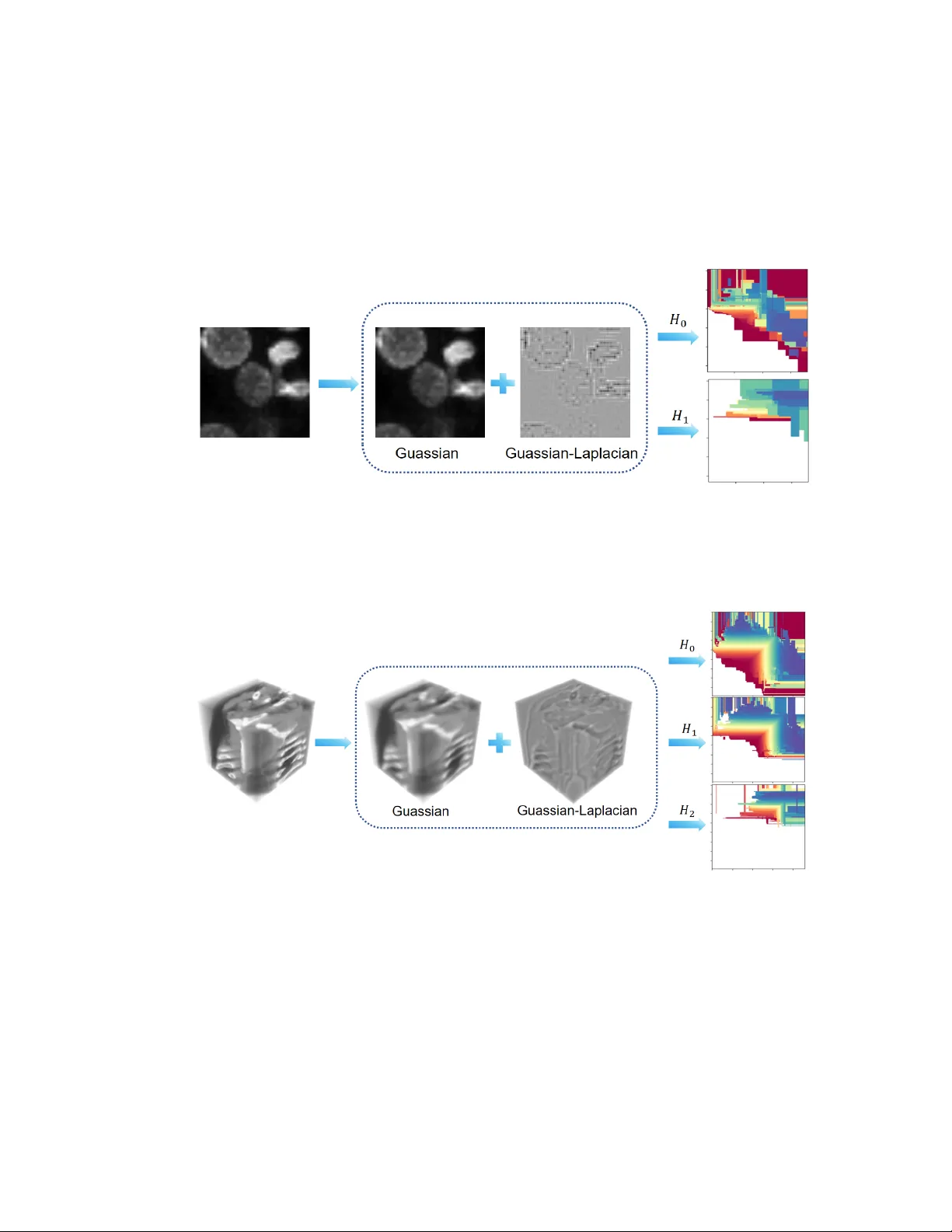
본 논문은 의료 영상 분석에 Topological Data Analysis(TDA)의 다중 파라미터 영속 동형학을 적용하기 위한 새로운 전처리 기법, G‑LoG 바이필터링을 제안한다. 기존 TDA는 Vietoris‑Rips, Čech, alpha, lower‑star 등 단일 파라미터 필터링에 의존해 왔으며, 다중 파라미터 접근은 주로 점군에 대한 복합 구조(예: Delaunay, rhomboid, subdivision)나 이미지 쌍을 이용한 특수 설계에 국한되었다. 의료 영상은 고차원 볼륨 데이터이며, 경계와 텍스처가 중요한 진단 정보를 담고 있기 때문에, 이러한 기존 방법만으로는 충분한 위상 정보를 추출하기 어렵다.
저자들은 먼저 의료 영상(2D 이미지 혹은 3D 볼륨)을 실수값 함수 φ:ℝⁿ→ℝ 로 모델링한다. 이후 Gaussian 커널 G와 그 라플라시안 ΔG를 이용해 두 개의 필터 함수 γ₁, γ₂를 정의한다. γ₁은 φ와 Gaussian 커널의 컨볼루션으로 얻어지는 스무딩된 이미지이며, γ₂는 φ와 ΔG의 컨볼루션으로 얻어지는 에지 강조 이미지이다. 수식적으로는
γ₁(x)=∫_{ℝⁿ} φ(x−α)·G(α)dα,
γ₂(x)=∫_{ℝⁿ} φ(x−α)·ΔG(α)dα.
이 두 함수는 각각 서브레벨 집합 X_{γ₁≤s}, X_{γ₂≤t}을 형성하고, (s,t)∈ℝ²에 대해 이중 파라미터 필터링을 만든다.
이론적 기여는 다음과 같다. (1) 정의된 G‑LoG 바이필터링이 연속 함수 공간 Φ 위에서 Lipschitz 연속성을 만족함을 보였다. 구체적으로, 두 함수 φ₁, φ₂에 대해 d_I(M(γ(φ₁)), M(γ(φ₂))) ≤ C·‖φ₁−φ₂‖∞ 가 성립한다. 여기서 C는 σ와 차원 n에 의존하는 상수이며, 증명 과정에서 Gaussian 적분과 ΔG의 2차 미분 항을 정밀히 계산했다. (2) 필터 함수가 “독립적”인 경우(예시 1.1) 다중 파라미터 영속 모듈이 두 단일 파라미터 모듈의 직접합으로 분해되어 위상 정보가 중복된다는 점을 이론적으로 설명한다. 따라서 γ₁과 γ₂가 교차하는 서브레벨 집합을 형성하도록 설계하는 것이 성능 향상의 전제조건이다.
실험은 MedMNIST v2 데이터셋을 사용했다. MedMNIST는 2D(예: PathMNIST, DermaMNIST)와 3D(예: OrganMNIST) 의료 이미지 서브셋을 포함하는 대규모 벤치마크이다. 각 이미지에 대해 G‑LoG 바이필터링을 적용하고, 얻어진 영속 모듈의 H₀, H₁(3D에서는 H₂) 바코드를 persistence image와 Betti curve 형태로 벡터화했다. 이후 이 벡터들을 입력으로 단일 은닉층 MLP(숨은 유닛 256)를 학습시켰으며, 학습 과정은 5‑fold 교차 검증으로 평가했다.
비교 대상은 다음과 같다. (a) 단일 파라미터 영속 동형학(오직 γ₁ 혹은 γ₂만 사용) 기반 MLP, (b) ResNet‑18/ResNet‑50, (c) AutoKeras, (d) auto‑sklearn, (e) Google AutoML Vision, (f) 최신 논문에서 제시된 Top‑Med(위상 특징을 결합한 하이브리드 모델). 결과는 G‑LoG 바이필터링 + MLP가 평균 정확도 86.3%를 기록, 단일 파라미터 영속 기반은 81.7%에 머물렀으며, ResNet‑50은 85.9%, AutoKeras 84.5%, Top‑Med 86.0% 수준이었다. 특히 3D OrganMNIST에서 G‑LoG + MLP가 84.1%를 달성, 3D CNN 기반 베이스라인(82.3%)보다 우수했다.
또한, 실험에서는 σ값을 1.0, 1.5, 2.0으로 변동시켰을 때 성능 변동이 미미함을 확인했으며, 이는 상수 C가 σ에 크게 의존하지 않음을 실증적으로 뒷받침한다.
논문의 의의는 다음과 같다. 첫째, 의료 영상에 직접 적용 가능한 이중 파라미터 필터링을 제시함으로써 TDA와 전통적인 이미지 전처리(Laplacian of Gaussian)를 자연스럽게 연결했다. 둘째, 영속 모듈 간의 interleaving distance가 입력 함수의 최대 노름에 대해 안정적이라는 이론적 보장을 제공함으로써, 실제 의료 데이터의 잡음·스캔 변동에 강인한 특성 추출이 가능함을 증명했다. 셋째, 복잡한 딥러닝 모델 없이도 위상 특징만으로 경쟁력 있는 분류 성능을 달성함으로써, 라벨링 비용이 높은 의료 현장에서 경량 모델 적용 가능성을 열었다.
한계점으로는 (1) 현재 실험이 MedMNIST라는 비교적 균일한 전처리와 라벨링을 가진 공개 데이터에 국한되어 있어, 실제 임상 CT·MRI·초음파 등 다양한 모달리티에 대한 일반화 검증이 부족하다. (2) 영속 특징을 벡터화하는 방법(예: persistence image 해상도, 가우시안 폭) 선택이 결과에 미치는 민감도 분석이 충분히 이루어지지 않았다. (3) G‑LoG 바이필터링 자체가 계산량이 큰 컨볼루션 연산을 포함하므로, 대규모 3D 볼륨에 대한 실시간 적용 가능성에 대한 논의가 부족하다.
향후 연구 방향은 (i) 멀티스케일 σ 자동 튜닝을 통해 다양한 해상도에서 동시에 정보를 추출하는 멀티‑스케일 G‑LoG를 설계하고, (ii) 영속 모듈을 그래프 신경망(GNN) 혹은 Transformer와 결합해 위상 정보와 지역 텍스처 정보를 동시에 학습하는 하이브리드 아키텍처를 탐색, (iii) 실제 임상 데이터셋(예: LIDC‑IDRI, BraTS)에서의 검증 및 모델 압축(프루닝, 양자화) 기법을 적용해 경량화된 의료 AI 솔루션을 구현하는 것을 제안한다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기