헬리컬 펩타이드 설계와 예측을 위한 조각별 적분 가능성
안내: 본 포스트의 한글 요약 및 분석 리포트는 AI 기술을 통해 자동 생성되었습니다. 정보의 정확성을 위해 하단의 [원본 논문 뷰어] 또는 ArXiv 원문을 반드시 참조하시기 바랍니다.
초록
이 논문은 단백질 백본을 이산형 비선형 슈뢰딩거 방정식(Discrete NLS)과 연결시키는 Hasimoto 변환을 활용한다. 전역적으로는 키랄(손잡이) 중복과 비국소 상호작용 때문에 제한이 있지만, 헬리컬 펩타이드 구간에서는 변환이 조각별로 적분 가능함을 보인다. 50개의 헬리컬 펩타이드 데이터를 분석해 이산 Hasimoto 지도와 이황성(다이헤드럴) 각 사이의 매핑을 정량화하고, Jacobian 조건수와 적분 오류 (E
상세 분석
본 연구는 단백질 구조를 수학적 적분계와 연결시키는 Hasimoto 지도(연속 경우는 곡률·비틀림을 복소수 파동함수로 변환)를 이산화한 형태, 즉 Discrete Hasimoto Map(DHM)을 헬리컬 펩타이드에 적용한다는 점에서 혁신적이다. 기존 연구에서는 DHM이 전체 단백질에 적용될 경우 키랄 중복(왼손·오른손 헬릭스가 동일한 파동함수로 매핑)과 장거리 상호작용 때문에 전역 적분성이 상실된다고 보고했다. 저자들은 이러한 한계를 “조각별 적분성(piecewise integrability)”이라는 개념으로 재구성한다.
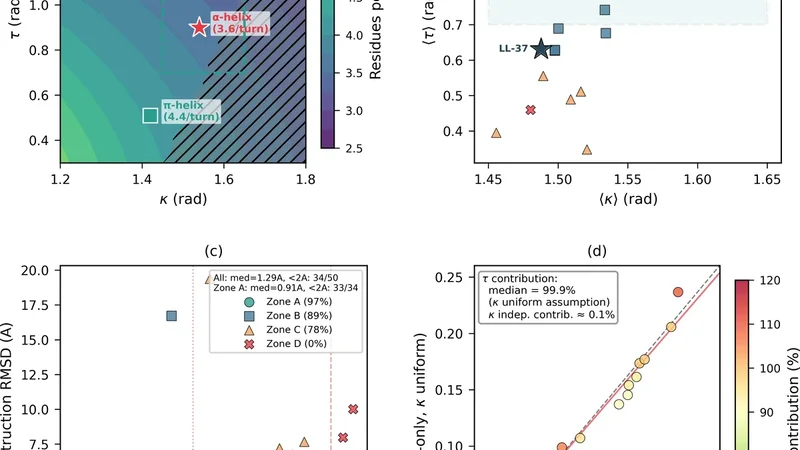
먼저 50개의 헬리컬 펩타이드(α‑helix, 3₁₀‑helix, π‑helix 등)를 선정하고, 각 잔기의 φ, ψ 이황성 각을 Frenet 프레임의 곡률 κ와 비틀림 τ로 변환한다. 변환식은
\
댓글 및 학술 토론
Loading comments...
의견 남기기