1,2프로판디올 이용 마이크로컴파트먼트의 실제 활성을 재해석하다
초록
Salmonella enterica LT2는 1,2‑프로판디올에 노출되면 Pdu 마이크로컴파트먼트를 형성한다. 기존 정제 MCP의 in vitro 활성을 in vivo 성장과 비교했을 때 큰 차이가 있었으며, 이는 세포 성장, 세포질에 존재하는 Pdu 연관 효소 및 비특이적 알코올 탈수소효소(PduQ 등)의 영향으로 해석된다. 저자들은 정제 MCP를 E. coli 용해액에 섞어 실험하고, PduQ를 제거한 LT2 균주로 성장 테스트를 수행해 이러한 가설을 검증하였다. 모델링 결과, PduCDE 복합체는 완전히 캡슐화되지만, 하류 효소들의 대부분은 세포질에서 작동한다는 새로운 in vivo 모델을 제시한다.
상세 분석
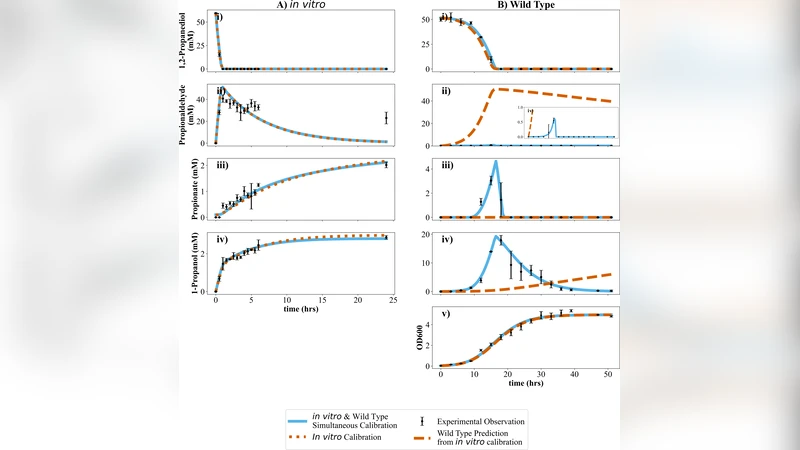
본 연구는 1,2‑프로판디올(PD) 이용 시 Salmonella enterica serovar Typhimurium LT2가 형성하는 Pdu 마이크로컴파트먼트(MCP)의 대사 활성을 정량적으로 비교·해석한다. 기존 문헌에서는 정제된 WT MCP를 in vitro에서 측정한 반응 속도가 실제 세포 내에서 관찰되는 성장 속도와 현저히 차이난다고 보고했으며, 이는 모델링을 통해 두 가지 주요 요인으로 귀결된다. 첫째, 살아있는 세포에서는 지속적인 성장과 물질 수송이 일어나며, 이는 효소 기질 접근성을 높여 전체 플럭스를 증가시킨다. 둘째, MCP 내부에 국한된 효소 외에도 MCP와 연관된 PduQ와 같은 알코올 탈수소효소가 세포질에 존재하여, PD의 산화와 아세틸‑CoA 생성에 기여한다. 정제 MCP는 이러한 세포질 효소와 물질 흐름을 배제하기 때문에 실제와는 다른 kinetic profile을 보인다.
저자들은 kinetic 모델을 구축하여 세포 성장률, 세포질 효소 활성도, 그리고 MCP 내부 효소의 캡슐화 정도를 변수로 설정하였다. 모델 시뮬레이션 결과, PduCDE 복합체(프로판디올 탈수소효소)는 완전히 MCP 내부에 격리되는 것이 가장 일관된 가정이며, 하류 단계인 PduP, PduL, PduQ 등은 세포질에 존재할 경우 전체 플럭스를 크게 증가시킨다. 특히 PduQ를 knockout한 LT2 균주에서 성장 속도가 현저히 감소함을 실험적으로 확인했으며, 이는 세포질 PduQ가 in vivo에서 중요한 보조 역할을 함을 시사한다.
또한, 정제 MCP를 E. coli 용해액에 첨가한 실험에서는 용해액 내 비특이적 알코올 탈수소효소가 MCP 내부 효소와 협동하여 PD 전환율을 높이는 현상이 관찰되었다. 이는 in vitro 실험에서 용해액을 포함시키면 세포질 효소 효과를 부분적으로 재현할 수 있음을 의미한다.
모델링 결과는 기존의 “모든 Pdu 효소가 MCP 내부에 캡슐화된다”는 가설을 수정한다. PduCDE는 반드시 MCP 내부에 위치해야 독성 중간체인 프로판디올 알데히드의 누출을 방지할 수 있지만, 하류 효소는 세포질에 존재해도 전반적인 대사 흐름에 큰 지장을 주지 않는다. 따라서 실제 세포에서는 MCP가 ‘반응 격리 구역’ 역할을 수행하면서도, 세포질 효소와의 협업을 통해 효율적인 1,2‑PD 이용이 이루어진다. 이러한 통합 모델은 MCP 기반 바이오엔지니어링 설계 시, 효소의 위치와 세포질 연계성을 고려해야 함을 강조한다.
댓글 및 학술 토론
Loading comments...
의견 남기기