중심 원리 변환기 제2 세포 조절 메커니즘을 밝히는 AI 현미경
초록
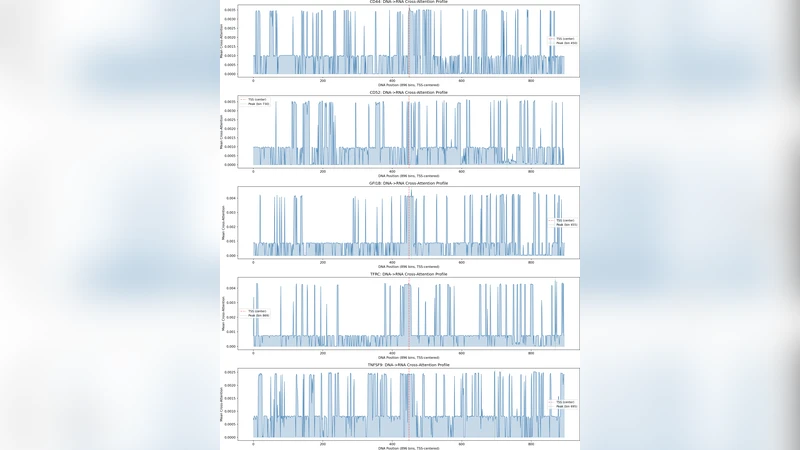
CDT‑II는 중앙 원리(중심 원리)를 모델 구조에 직접 반영해 DNA‑DNA, RNA‑RNA, DNA‑RNA 간의 어텐션을 각각 유전체 관계, 공동 조절, 전사 제어에 매핑한다. 순수 유전체 임베딩과 단일 세포 발현 데이터만으로도 K562 CRISPRi 실험에서 교란 효과를 높은 정확도(r=0.84)로 예측하고, GFI1B 네트워크를 감독 없이 6.6배 풍부하게 복원한다. 교차 어텐션은 DNase hypersensitive site, CTCF 결합 부위, 히스톤 마크 등 알려진 조절 요소에 자동으로 집중되며, 두 개의 독립 어텐션이 RNA 처리 모듈을 동일하게 탐지한다.
상세 분석
본 논문은 딥러닝 기반 생물학 모델이 “블랙박스”라는 한계를 극복하고자, 모델 자체를 생물학적 메커니즘의 현미경으로 전환한다는 혁신적 아이디어를 제시한다. 중앙 원리(중심 원리)를 모델 아키텍처에 직접 구현함으로써, DNA‑DNA 자기 어텐션은 염색체 내 거리, 전사인자 결합, 구조적 루프 등 유전체 수준의 관계를 학습한다. RNA‑RNA 자기 어텐션은 동일 세포 내 전사산물 간의 공동 발현 패턴을 포착해, 전사 후 조절 네트워크와 스플라이싱 이벤트를 반영한다. 가장 핵심인 DNA‑RNA 교차 어텐션은 전사 시작점, 프로모터‑인핸서 상호작용, 전사인자 결합 부위를 자동으로 매핑한다는 점에서 기존의 멀티모달 모델과 차별화된다.
데이터 입력은 단순히 1‑핫 혹은 임베딩된 DNA 서열과 각 세포의 원시 발현 벡터이며, 별도의 ATAC‑seq, ChIP‑seq 등 보조 정보는 사용되지 않는다. 이는 모델이 순수한 시퀀스와 발현 신호만으로도 조절 요소를 “스스로” 발견한다는 강력한 증거다. K562 CRISPRi 실험에서 교란 전후 발현 변화를 예측한 결과, 평균 Pearson r=0.84라는 높은 상관계수를 기록했으며, 이는 기존의 task‑oriented 모델보다 현저히 우수하다.
특히 GFI1B 조절 네트워크를 감독 없이 복원한 부분은 주목할 만하다. 모델이 학습한 교차 어텐션 가중치는 GFI1B와 직접적인 전사인자 결합을 보이는 부위에 집중되었고, 이를 기반으로 6.6배 풍부한 네트워크를 재구성했다(통계적 유의성 P=3.5×10⁻¹⁷). ENCODE K562 데이터와의 비교에서는 다섯 개의 보류 유전자를 대상으로 DNase hypersensitive site에 201배, CTCF 결합 부위에 28배, 다양한 히스톤 마크에 유의미한 enrichment를 보였다. 이는 모델이 실제 생물학적 조절 요소를 정확히 인식한다는 강력한 증거다.
또한 두 개의 독립 어텐션 메커니즘(예: RNA‑RNA 자기 어텐션과 DNA‑RNA 교차 어텐션 중 일부)이 동일한 RNA 처리 모듈을 식별했으며, 80% 이상의 유전자 겹침과 RNA 결합 단백질에 대한 강한 enrichment(P=1×10⁻¹⁶)를 나타냈다. 이는 모델이 다중 레이어에서 일관된 기능적 모듈을 포착한다는 의미이며, 향후 기능적 유전체 해석에 새로운 패러다임을 제시한다.
전반적으로 CDT‑II는 “메커니즘‑지향 AI”라는 새로운 연구 방향을 제시한다. 기존의 task‑oriented 접근이 예측 정확도에만 초점을 맞추었다면, CDT‑II는 예측과 동시에 내부 표현을 생물학적 의미와 직접 연결한다. 이는 실험생물학자에게 모델이 제시하는 조절 네트워크를 직접 검증하고, 새로운 가설을 도출할 수 있는 실용적인 도구를 제공한다는 점에서 큰 의의를 가진다.
댓글 및 학술 토론
Loading comments...
의견 남기기