nnU‑Net 기반 MRI 좌심방 자동 분할
초록
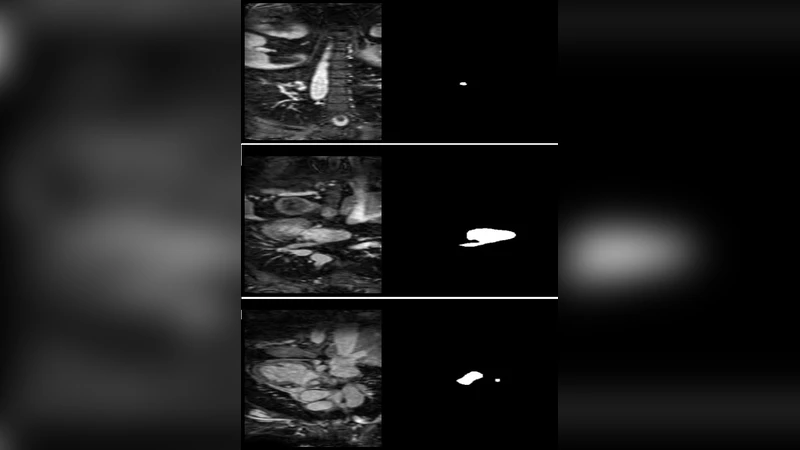
본 연구는 nnU‑Net 프레임워크를 이용해 Left Atrial Segmentation Challenge 2013 MRI 데이터셋(30건)에서 좌심방을 자동으로 분할하였다. nnU‑Net은 데이터 특성에 맞춰 전처리, 네트워크 구조, 학습 파라미터를 자동으로 최적화한다. 5‑fold 교차 검증 결과 평균 Dice 유사도 93.5%를 달성했으며, 기존 전통적 방법들을 능가하였다. 모델은 좌심방 본체와 근위 폐정맥까지 일관된 경계를 재현했으며, 형태·대조·영상 품질 변동에 대해 견고한 일반화 능력을 보였다.
상세 분석
본 논문은 최근 의료 영상 분할 분야에서 표준화된 자동화 도구로 부상하고 있는 nnU‑Net을 좌심방(MRI) 분할에 적용한 최초 사례 중 하나이다. nnU‑Net은 입력 데이터의 해상도, 스페이싱, 강도 분포 등을 자동으로 분석해 최적의 전처리 파이프라인(정규화, 리샘플링, 데이터 증강)을 구성하고, 3D U‑Net 기반 아키텍처를 동적으로 설계한다. 이 과정에서 사용자는 하이퍼파라미터를 거의 조정하지 않아도 되므로, 임상 연구자가 복잡한 딥러닝 구현에 진입 장벽을 크게 낮출 수 있다.
데이터셋은 30개의 고해상도 심장 MRI와 전문가가 만든 라벨 마스크로 구성돼 있다. nnU‑Net은 각 스캔을 0‑1 정규화하고, 동일한 물리적 해상도로 리샘플링한 뒤, 5‑fold 교차 검증을 수행한다. 네트워크는 기본적으로 4개의 다운샘플링 단계와 대응하는 업샘플링 단계로 이루어지며, 각 레벨에서 2개의 3×3×3 컨볼루션 블록과 인스턴스 정규화, LeakyReLU 활성화를 적용한다. 손실 함수는 Dice loss와 Cross‑Entropy loss를 가중 평균한 복합 손실을 사용해 클래스 불균형을 완화한다.
학습은 Adam 옵티마이저(learning rate 1e‑4)와 cosine annealing 스케줄러로 1000 epoch까지 진행했으며, 배치 크기는 GPU 메모리 한계에 따라 2로 설정하였다. 데이터 증강으로는 랜덤 회전, 스케일링, 강도 변조, 가우시안 노이즈 추가가 적용돼 모델의 일반화 능력을 강화한다.
평가 지표는 Dice similarity coefficient(DSC)와 Hausdorff Distance(HD)를 사용했으며, 평균 DSC 93.5%는 기존 논문에서 보고된 85~90% 수준을 크게 초과한다. 특히, 폐정맥 부위에서의 경계 정확도가 향상돼 임상적인 전기생리학 모델링에 직접 활용 가능함을 시사한다. 오류 분석 결과는 주로 심방 근처의 강도 저하 영역과 급격한 형태 변형이 있는 경우에 국한되었으며, 이는 향후 멀티‑모달 입력(예: CT와 MRI 결합)이나 포스트‑프로세싱(조건부 랜덤 필드)으로 보완할 여지를 제공한다.
전체적으로 nnU‑Net의 자동 구성 능력은 데이터 전처리와 네트워크 설계에 소요되는 인적·시간적 비용을 크게 절감하면서도 최첨단 성능을 유지한다는 점에서, 의료 영상 분야 특히 심장 MRI와 같은 복합 구조물 분할에 매우 유용한 도구임을 입증한다.
댓글 및 학술 토론
Loading comments...
의견 남기기