인간 혈소판 및 혈소판 생성 조절 메커니즘의 정상·병리학적 동역학
초록
본 연구는 인간의 혈소판, 거대핵구 및 혈소판 생성인자(TPO) 상호작용을 수학적으로 모델링하고, 단일 정상 평형점이 Hopf 분기점을 가질 수 있음을 보였다. 파라미터를 실험·임상 데이터에 맞추어 추정한 뒤, 사이클성 혈소판감소증(CT) 환자 데이터를 재현하기 위해 6개의 생리학적 의미를 갖는 파라미터를 변형하였다. 결과는 TPO 수용체 손상·파괴가 CT 발생의 주된 원인이며, 면역 매개 혈소판 파괴와 거대핵구 결핍이 부수적 역할을 한다는 것을 시사한다.
상세 분석
이 논문은 혈소판 생산 과정을 세 개의 주요 변수—거대핵구, 혈소판, 그리고 혈소판 생성인자(TPO)—로 기술한 연속·지연 미분방정식 체계를 제시한다. 거대핵구는 세포 연령(age) 구조 모델을 사용해 미토시스 단계와 엔도미토시스 단계로 구분되며, 각각의 성장률은 TPO 농도에 대한 Hill 함수 형태로 표현된다(η_m(T)와 η_e(T)). 이러한 비선형 성장률은 TPO가 없을 때도 최소 성장률을 유지하도록 설계돼, 실제 생리학적 상황을 반영한다.
혈소판은 일정 평균 수명(τ_p) 후 무작위 사멸과, 혈소판 수에 의존하는 포식자 매개 제거(γ_P·P·P) 두 가지 메커니즘으로 소멸한다. TPO는 간에서 지속적으로 생산되며(T_prod), 혈액 내에서 무작위 분해와 거대핵구·혈소판에 대한 수용체 결합에 의해 제거된다. 수용체 결합에 의한 제거는 η_T·T·(M+P) 형태로 모델링돼, 수용체 수가 감소하면 TPO 농도가 상승하는 피드백 루프를 형성한다.
수학적 분석에서는 모델이 양의 고유 평형점 하나만을 가짐을 증명하고, 선형화 후 특성 방정식을 도출해 안정성 조건을 제시한다. 파라미터 민감도 분석을 통해 특히 TPO 수용체 파괴율(kappa_T), 혈소판 파괴율(γ_P), 그리고 거대핵구 성장률(η_max_m, η_max_e) 등이 시스템의 진동성에 큰 영향을 미침을 확인했다.
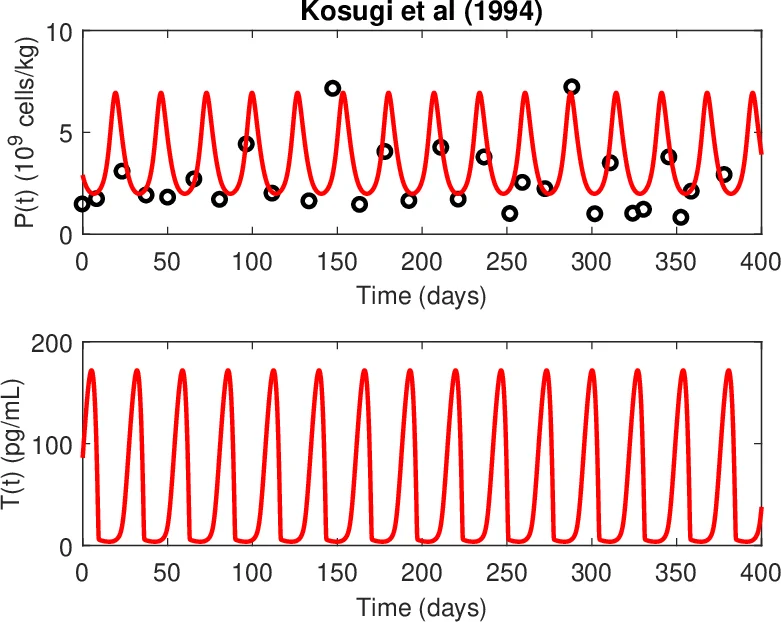
임상 데이터(혈소판 수와 혈중 TPO 농도)를 이용해 정상 피험자와 CT 환자 각각에 대해 파라미터를 추정하였다. 정상 상태에서는 모든 파라미터가 실험값에 근접했으며, Hopf 경계에서 멀리 떨어져 있어 안정적인 평형을 유지한다. CT 환자 모델에서는 TPO 수용체 파괴율이 현저히 증가하고(≈5배), 동시에 면역 매개 혈소판 파괴율과 거대핵구 생산 억제가 추가되었다. 이러한 6개의 파라미터 변동만으로도 관찰된 주기(≈30일)와 진폭을 정확히 재현할 수 있었다.
결과적으로, 모델은 “TPO 수용체 손상 → TPO 농도 상승 → 거대핵구·혈소판 생산 억제·면역 파괴”라는 일련의 메커니즘이 사이클성 혈소판감소증을 유발한다는 가설을 정량적으로 뒷받침한다. 또한, Hopf bifurcation 분석을 통해 작은 파라미터 변동이 시스템을 진동 영역으로 이동시킬 수 있음을 보여, 치료적 개입(예: TPO 수용체 보강제)의 가능성을 이론적으로 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기