딥 뉴럴 네트워크를 활용한 의료 영상 정합 종합 리뷰
초록
본 논문은 의료 영상 정합 분야에 딥 뉴럴 네트워크(DNN)를 적용한 최신 연구들을 체계적으로 정리한다. 정합 문제의 복잡성을 설명하고, 지도·비지도·약지도 학습 방식, 주요 손실 함수, 데이터셋 및 평가 지표 등을 분류·분석한다. 또한 현재 직면한 데이터 부족, 도메인 차이, 해석 가능성 등의 도전 과제와 트랜스포머 기반 모델, 연합 학습, 멀티모달 정합 등 향후 연구 방향을 제시한다.
상세 분석
논문은 먼저 의료 영상 정합이 “이미지‑이미지 매핑”이라는 근본적인 문제를 해결하기 위해 변형 파라미터(변형장, 매트릭스 등)를 추정하는 과정이며, 전통적인 최적화 기반 방법은 계산량이 크고 지역 최소값에 빠지기 쉬운 한계를 가지고 있음을 지적한다. 이러한 한계를 극복하기 위해 최근 GPU와 대규모 데이터셋을 활용한 딥 뉴럴 네트워크(DNN) 기반 접근법이 급부상했으며, 저자는 이를 크게 세 가지 학습 패러다임—지도 학습, 비지도 학습, 약지도 학습—으로 구분한다.
지도 학습 방식은 합성 변형을 이용해 정답 변형장을 생성하고, 네트워크가 이를 직접 회귀하도록 훈련한다. 대표적인 모델로 VoxelMorph‑Supervised, DeepReg 등이 있으며, L2 손실, 정규화 손실, 변형장 스무딩 손실을 결합해 정확도와 변형의 물리적 일관성을 동시에 확보한다. 그러나 라벨(정답 변형장) 확보가 비용이 많이 들고, 실제 임상 변형과의 차이가 발생할 위험이 있다.
비지도 학습은 변형 파라미터를 직접 예측한 뒤, 변환된 움직이는 이미지와 고정 이미지 사이의 유사도(예: NCC, MI, SSIM)를 최소화하는 방식이다. 여기서 핵심은 차별화 가능한 유사도 함수와 변형장 정규화(스무딩, 디버깅) 손실을 어떻게 설계하느냐이다. VoxelMorph‑Unsupervised, DIR‑Net, PDD-Net 등이 대표적이며, 특히 다중 스케일 피라미드 구조와 순환형 네트워크를 도입해 큰 변형도 효율적으로 학습한다.
약지도 학습은 부분적인 라벨(예: 해부학적 랜드마크, 세그멘테이션 마스크)만을 이용해 손실을 구성한다. 이 접근법은 라벨 비용을 크게 낮추면서도 정합 정확도를 유지한다. 대표적인 연구로는 라벨‑프리 정합을 위한 Cycle‑GAN 기반 프레임워크와, 랜드마크 기반 정합을 위한 Heatmap‑Regression 네트워크가 있다.
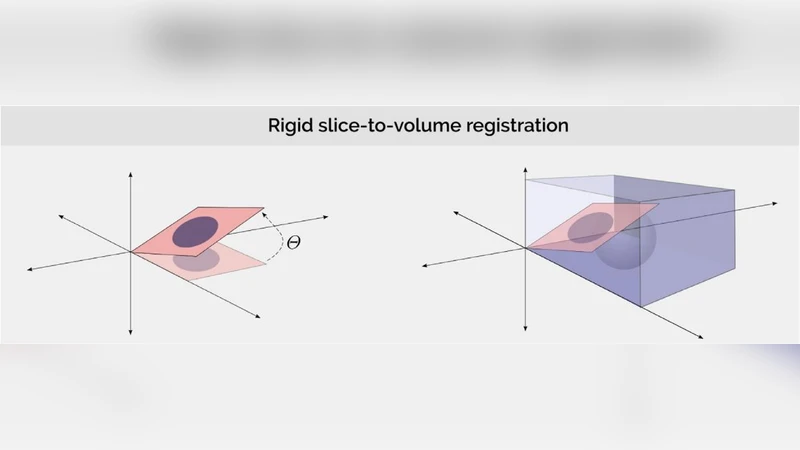
데이터 측면에서 저자는 공개 데이터셋(IXI, OASIS, ADNI, MNI, LUNA 등)과 자체 구축 데이터셋을 비교 분석하고, 데이터 전처리(강도 정규화, 해부학적 정렬)와 데이터 증강(랜덤 변형, 가우시안 노이즈) 전략이 모델 일반화에 미치는 영향을 정량화한다. 특히, 3D 볼륨 입력에 대한 메모리 제약을 해결하기 위해 슬라이스‑기반 2D CNN, 하이브리드 2.5D 구조, 그리고 최근의 메모리 효율적인 트랜스포머(예: Swin‑UNet) 등을 활용한 사례를 제시한다.
성능 평가에서는 Dice 계수, Hausdorff 거리, 평균 표면 거리(MSD) 등 정량적 지표와 시각적 정합 품질을 동시에 고려한다. 통계적 분석 결과, 비지도 모델이 지도 모델에 비해 평균 Dice가 2~3% 낮지만, 라벨 비용이 0에 가까워 실용적 가치가 높다. 또한, 멀티모달 정합(CT‑MRI, PET‑MRI)에서는 도메인 적응 기법(Adversarial Loss, Cycle‑Consistency)과 사전 학습된 백본(ResNet, EfficientNet) 사용이 성능 향상에 크게 기여한다.
도전 과제로는 (1) 데이터 스케일링 문제—대규모 3D 볼륨을 효율적으로 학습시키는 하드웨어·알고리즘 최적화, (2) 도메인 차이—다양한 스캐너·프로토콜에 대한 일반화, (3) 해석 가능성—변형장의 물리적 의미와 임상적 신뢰성 확보, (4) 실시간 적용—수술 중 실시간 정합을 위한 경량화 모델과 하드웨어 가속이 필요함을 강조한다.
미래 연구 방향으로는 (i) 자기지도 학습 및 대규모 비라벨 데이터 활용, (ii) 트랜스포머 기반 전역 컨텍스트 모델링, (iii) 연합 학습을 통한 개인정보 보호와 데이터 다양성 확보, (iv) 멀티모달·멀티스케일 통합 정합 프레임워크, (v) 정합 결과의 불확실성 추정 및 임상 의사결정 지원 시스템과의 연계 등을 제시한다. 이러한 흐름은 의료 영상 정합을 단순한 이미지 매핑을 넘어, 정밀 의료와 인공지능 기반 진단·치료 파이프라인의 핵심 구성 요소로 자리매김하게 할 것으로 전망한다.
댓글 및 학술 토론
Loading comments...
의견 남기기