Ti‑6Al‑4V 합금의 생리학적 용액 내 전기화학적 거동: 단백질 함량과 시간‑주파수 분석에 관한 연구
초록
본 연구는 Ti‑6Al‑4V 합금을 다양한 생리학적 용액(리거, PBS, PBS + 알부민, PBS + 소혈청, PBS + 소혈청 + 아지드) 및 초순수 물에서 전기화학 임피던스 분광법(EIS)으로 평가하였다. 시간‑주파수‑모듈 그래프를 통해 재현성 및 보호 효과를 분석했으며, 초순수 물이 가장 보호성이 높고, PBS + 알부민이 가장 부식에 취약함을 확인하였다. 또한 유기·무기 종의 흡착 특성을 그래픽 서명으로 구분하였다.
상세 분석
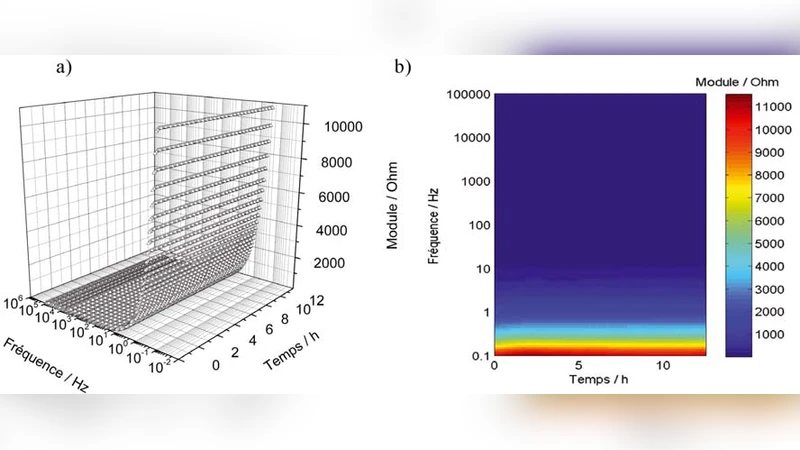
이 논문은 Ti‑6Al‑4V 합금이 인체 내 임플란트 재료로 사용될 때, 주변 체액에 포함된 단백질 및 기타 생리학적 성분이 전기화학적 부식 거동에 미치는 영향을 정량적으로 규명하고자 한다. 실험은 전통적인 전위‑전류 측정 대신, 넓은 주파수 범위(10 mHz ~ 100 kHz)를 커버하는 전기화학 임피던스 분광법(EIS)을 채택하였다. EIS 데이터는 복소 임피던스 Z*를 실부와 허부로 분리하고, 이를 시간‑주파수‑모듈( |Z| ) 그래프로 변환함으로써, 각 용액에서의 보호막 형성 및 성장 과정을 시각화하였다.
재현성 평가는 동일 조건 하에 5회 반복 측정을 수행하고, 각 실험군의 |Z| 평균값과 표준편차를 비교함으로써 수행되었다. 결과는 초순수 물에서 가장 낮은 변동성을 보였으며, 이는 전해질 자체가 거의 반응하지 않아 실험적 잡음이 최소화된다는 것을 의미한다. 반면, PBS + 알부민 용액은 |Z| 값이 크게 감소하고 변동폭이 확대되어, 알부민이 티타늄 표면에 흡착하면서 보호막을 얇게 만들거나 불균일하게 형성함을 시사한다.
PBS + 소혈청(칼프 혈청) 용액에서는 알부민 외에도 다양한 혈청 단백질(글로불린, 피브리노겐 등)이 존재한다. 이들 단백질은 복합적인 흡착층을 형성해 전기화학적 저항을 어느 정도 회복시키지만, 여전히 초순수 물에 비해 보호성이 낮다. 흥미롭게도, 동일 용액에 항산화제인 아지드(나트륨 아지드)를 첨가했을 때는 |Z| 평균이 약간 상승했으며, 이는 자유 라디칼에 의한 부식 진행을 억제하는 효과를 나타낸다.
시간‑주파수‑모듈 그래프는 특히 저주파 영역(≤1 Hz)에서 큰 차이를 보였는데, 이는 전하 전달 저항(R_ct)과 용액 저항(R_s)의 변화를 반영한다. 고주파 영역(≥10 kHz)에서는 용량성 요소(C_dl)의 변동이 두드러졌으며, 이는 표면에 형성된 전기 이중층의 두께와 구조가 용액 성분에 따라 달라짐을 의미한다. 이러한 그래프상의 ‘서명’은 유기(단백질)와 무기(이온) 종의 흡착을 구분하는 데 유용하며, 향후 임플란트 표면 개질 전략 수립에 활용될 수 있다.
전반적으로, 이 연구는 EIS와 시간‑주파수 분석을 결합함으로써 복합적인 생리학적 환경에서 Ti‑6Al‑4V 합금의 부식 메커니즘을 정량적으로 파악하고, 단백질 함량이 보호막 형성에 미치는 부정적 영향을 명확히 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기