뇌종양 분할을 위한 3D U‑Net에 병변 사전 정보 통합
본 논문은 BraTS 2017 데이터셋을 이용해, 다중 모달 MRI와 병변 사전(VOI) 맵을 결합한 13채널 입력을 3D U‑Net에 적용함으로써 기존 3D U‑Net 대비 향상된 Dice와 Hausdorff 지표를 달성한 방법을 제시한다. VOI 맵은 훈련 데이터의 라벨을 MNI 표준공간에 정합한 뒤, 각 병변 유형(ED, NCR/NET, ET)의 히트맵을 생성하고, 백분위 기반 임계값을 이용해 0~9 레이블로 구분한다. 이 사전 정보를 M…
저자: Po-Yu Kao, Jefferson W. Chen, B.S. Manjunath
본 논문은 뇌종양 자동 분할에서 기존 3D U‑Net에 병변 사전 정보를 효과적으로 결합하는 새로운 접근법을 제안한다. 연구 배경으로는 뇌종양이 위치적 특성을 가지고 있음에도 불구하고, 대부분의 딥러닝 기반 분할 모델은 이미지 강도와 텍스처에만 의존한다는 점을 들었다. 이를 보완하기 위해 저자들은 BraTS 2017 데이터셋(285개의 훈련, 46개의 검증)을 활용해 병변 사전(VOI) 맵을 구축하였다.
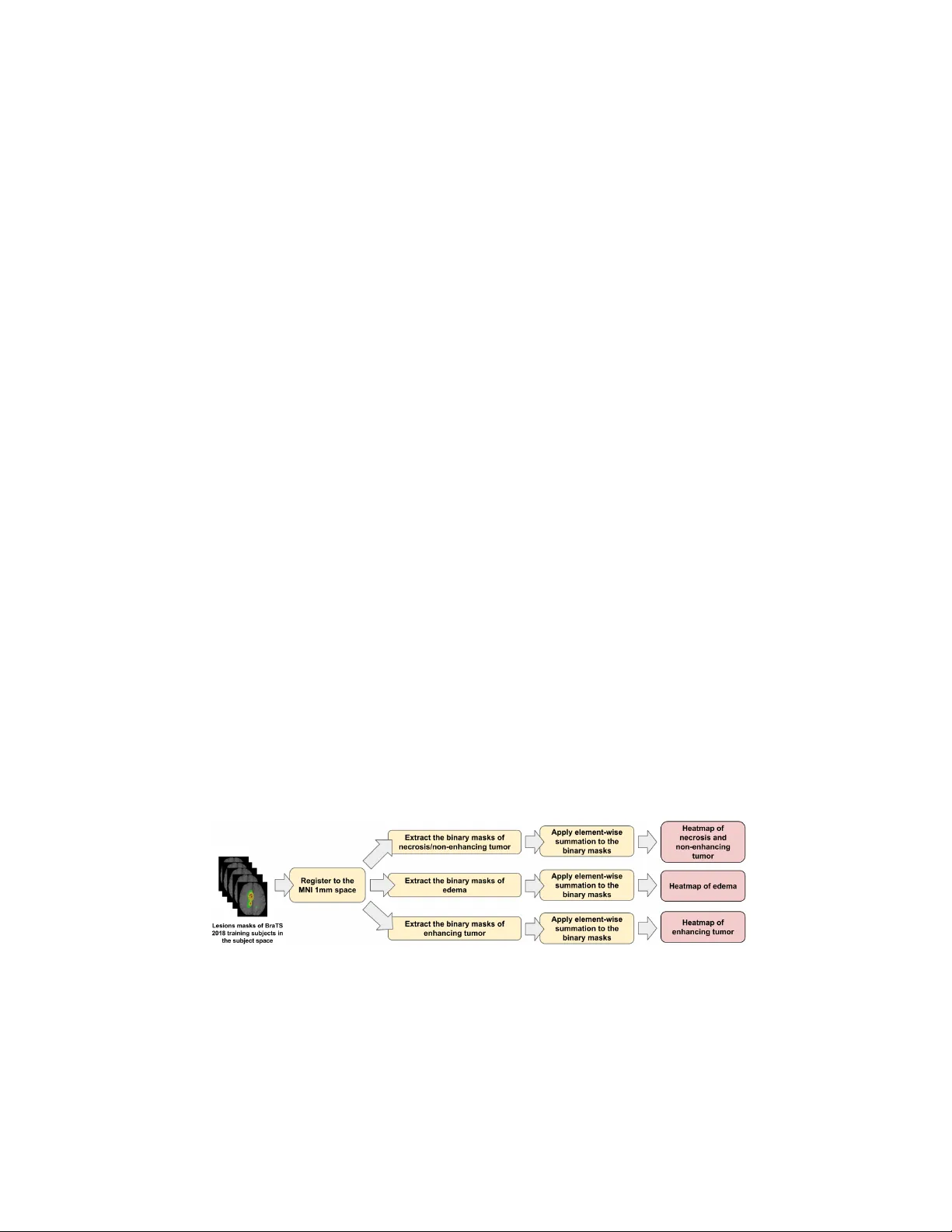
VOI 맵 구축 과정은 다음과 같다. 첫째, 각 환자의 라벨(ED, NCR/NET, ET)을 MNI 1 mm 표준공간에 FLIRT를 이용해 정합한다. 둘째, 정합된 라벨을 3가지 이진 마스크로 분리하고, 모든 환자에 대해 voxel‑wise 합산해 각 병변 유형별 히트맵을 만든다. 셋째, 히트맵의 비제로 voxel 빈도수를 내림차순 정렬하고, 50 %, 65 %, 80 % 백분위값을 각각 h_ed, h_ncr, h_et 로 정의한다. 넷째, 알고리즘 1에 명시된 계층적 우선순위 규칙을 적용해 각 voxel에 0~9 레이블을 할당한다. 여기서 레이블 9는 ET가 가장 높은 확률을 가질 때, 8은 NCR/NET, 7은 ED가 높은 확률을 가질 때 부여되며, 하위 레벨에서는 각각의 백분위 임계값을 순차적으로 적용한다. 최종 VOI 맵은 10개의 레이블(0‑9)로 구성된다.
생성된 VOI 맵은 각 환자의 원본 MRI(4채널: T1, T1‑c, T2, FLAIR)와 동일한 해상도로 역정합된 뒤, 9개의 바이너리 채널(각 레이블별)로 분리된다. 이 9채널과 MRI 4채널을 결합해 13채널 입력을 만든다. 네트워크는 기존 3D U‑Net 구조를 그대로 사용하되, 모든 합성곱 층에 Group Normalization(4 groups)과 0.3 dropout을 적용하고, 업샘플링은 trilinear interpolation을 사용한다.
학습은 128³ 크기의 랜덤 패치를 배치 사이즈 2로 300 epoch 동안 진행한다. 옵티마이저는 Adam(초기 학습률 1e‑3)과 AMSGrad, L2 정규화(1e‑4)를 사용한다. 손실 함수는 다클래스 교차 엔트로피에 hard‑negative mining을 적용해, 손실이 큰 배경 voxel 중 상위 3배만 역전파에 포함시킨다. 데이터 증강은 적용하지 않았다. 테스트 시에는 전체 240×240×155 볼륨을 그대로 입력한다. 훈련 시간은 약 12.5시간, 테스트는 1.5초(1080 Ti GPU)이다.
성능 평가는 Dice similarity coefficient와 95th percentile Hausdorff distance(H95)를 사용했다. 실험 결과, VOI 맵을 추가한 단일 3D U‑Net은 ET Dice가 0.695→0.730(+3.5%), ET H95가 6.79→4.23 mm(‑2.56 mm)로 크게 향상되었다. 전체 종양(Whole Tumor)과 종양 코어(Tumor Core)에서도 소폭 개선이 관찰되었다. 5‑model 앙상블에서도 동일한 경향이 나타났으며, ET Dice가 0.723→0.744(+2.1%), TC Dice가 0.763→0.780(+1.7%)로 상승했다.
비교 대상인 Isensee et al.와 Kamnitsas et al.의 최신 모델과도 경쟁 가능한 성능을 보였다. 특히 Kamnitsas 팀은 7가지 서로 다른 모델을 앙상블했음에도 불구하고, 저자들의 5‑model 앙상블이 비슷하거나 더 나은 Dice와 H95를 기록했다. 이는 복잡한 모델 설계 없이도 사전 정보를 제공함으로써 성능을 끌어올릴 수 있음을 증명한다.
논문의 한계로는 VOI 맵이 훈련 데이터에 기반한다는 점이다. 새로운 데이터셋이나 병변 유형이 추가될 경우, 히트맵을 재구축해야 하며, 정합 오류가 있을 경우 성능 저하가 발생할 수 있다. 또한 데이터 증강을 사용하지 않아 일반화 능력이 제한될 가능성이 있다. 향후 연구에서는 다기관 데이터에 대한 도메인 적응, 정합 자동화, 그리고 Transformer 기반 네트워크와의 결합 등을 통해 사전 정보 활용을 확대할 수 있을 것이다.
결론적으로, 본 연구는 병변 사전(VOI) 맵을 3D U‑Net에 통합함으로써 뇌종양 분할 성능을 실질적으로 향상시켰으며, 이 접근법은 다른 네트워크 아키텍처에도 손쉽게 적용 가능함을 보여준다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기