전체 슬라이드 세포병리 이미지 기반 갑상선암 악성도 예측
초록
본 논문은 초고해상도 전체 슬라이드 세포병리 이미지에서 갑상선암의 악성 여부와 Bethesda 점수를 동시에 예측하는 두 단계 딥러닝 파이프라인을 제안한다. 첫 단계는 전문가가 라벨링한 소수의 패치를 이용해 갑상선 세포 군을 식별하고, 두 번째 단계는 식별된 영역을 집계해 전 슬라이드 수준의 악성도와 TBS 카테고리를 예측한다. 908장의 데이터셋을 구축하고, 109장의 독립 테스트 슬라이드에서 인간 전문가와 동등한 성능을 보이며, 특히 TBS 2·6에 대해 100% 정확도를 달성했다.
상세 분석
이 연구는 전통적인 다중 인스턴스 학습(MIL) 접근법이 전체 슬라이드에서 극히 드문 진단 영역을 효과적으로 활용하지 못한다는 점을 지적한다. 이를 해결하기 위해 저자들은 두 단계의 컨볼루션 신경망(CNN) 구조를 설계했으며, 첫 번째 네트워크는 VGG11 기반으로 설계돼 전문가가 직접 라벨링한 5,461개의 follicular cell cluster 패치를 학습한다. 이 단계는 ‘배경’(혈액 세포, 잡음)과 ‘진단 영역’(갑상선 세포 군)을 명확히 구분하도록 지도학습을 적용함으로써, 기존 MIL에서 흔히 발생하는 잡음 감소 문제를 근본적으로 해결한다.
두 번째 네트워크는 첫 단계에서 추출된 진단 영역들의 특징을 집계하여 슬라이드 전체의 악성도(Y∈{0,1})와 Bethesda 점수(S∈{2,3,4,5,6})를 동시에 예측한다. 여기서 핵심은 하나의 실수형 출력값을 여러 임계값과 비교해 순서형 회귀(ordinal regression)를 수행한다는 점이다. 즉, 모델은 단일 스칼라를 출력하고, 이를 사전 정의된 임계값에 매핑해 TBS 카테고리를 결정함으로써, 카테고리 간 순서 관계를 자연스럽게 보존한다. 이러한 설계는 TBS 점수가 악성도와 강한 단조성을 갖는 임상적 사실을 모델에 직접 반영하게 하여, 예측 정확도를 향상시키는 정규화 역할을 한다.
데이터 전처리 측면에서 저자들은 150,000 × 100,000 픽셀 규모의 초고해상도 슬라이드를 4배 다운샘플링하고, 자동 초점 중심 평면만을 사용해 메모리와 연산 부담을 크게 낮췄다. 또한, 전체 908장의 슬라이드 중 142장을 선택해 전문가가 직접 영역을 라벨링함으로써, 라벨링 비용을 최소화하면서도 충분한 양의 양성 샘플을 확보했다.
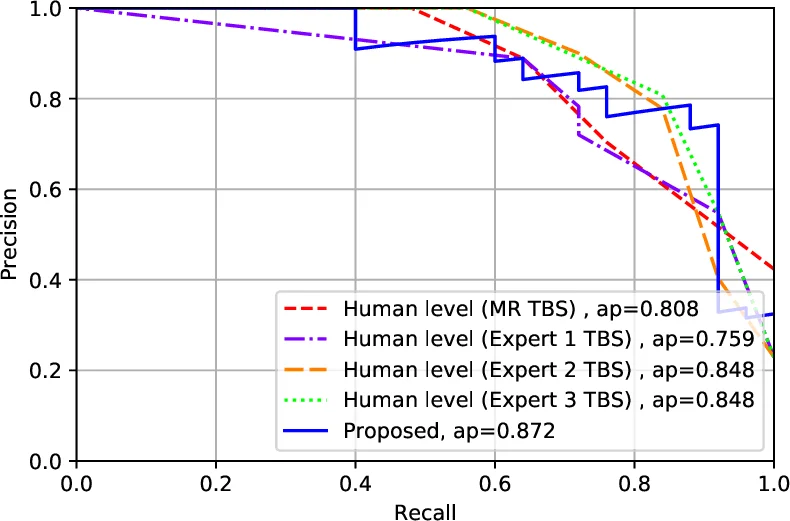
실험 결과는 109장의 독립 테스트 슬라이드에서 모델이 3명의 독립 병리전문의와 동등한 AUC를 기록했으며, 특히 TBS 2와 6에 대해 100% 정확도를 달성했다는 점에서 임상 적용 가능성을 크게 시사한다. 모델이 TBS 3~5와 같은 ‘불확정’ 카테고리를 정확히 구분해 악성 가능성을 재평가함으로써, 기존 진단에서 발생할 수 있는 과잉 수술이나 불필요한 추적 검사를 감소시킬 수 있다.
이 논문의 주요 기여는 (1) 전체 슬라이드에서 진단 영역을 효과적으로 추출하기 위한 지도학습 기반 검출기, (2) 악성도와 Bethesda 점수를 동시에 예측하는 순서형 회귀 설계, (3) 대규모 초고해상도 데이터셋 구축 및 실험을 통한 인간 전문가 수준의 성능 입증이다. 향후 연구에서는 다중 초점 스택을 활용한 3D 정보 통합, 더 깊은 네트워크 구조 적용, 그리고 다른 종류의 세포병리 이미지로의 일반화 가능성을 탐색할 여지가 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기