다중 시퀀스 MRI 기반 뇌 전이병 자동 검출·분할 딥러닝
초록
본 연구는 1.5T·3T 다중 시퀀스 3D MRI 데이터를 이용해, GoogLeNet 기반 2.5D 완전합성곱 신경망(CNN)으로 뇌 전이병을 자동 검출·분할하는 방법을 제시한다. 156명의 환자(100명 훈련, 5명 개발, 51명 테스트)에서 전처리·라벨링을 수행했으며, 테스트군은 병변 수에 따라 1‑3개, 4‑10개, 10개 초과 세 그룹으로 나누었다. 전체 AUC는 0.98(그룹별 0.99/0.97/0.97)이며, 최적 임계값에서 정밀도 0.79, 재현율 0.53, Dice 0.79를 기록했다. 평균 위양성은 환자당 8.3개(전체)·3.4개(10 mm³ 이상)였다. 결과는 다중 시퀀스 MRI와 딥러닝 결합이 뇌 전이병 검출·분할에 실질적 보조가 될 수 있음을 보여준다.
상세 분석
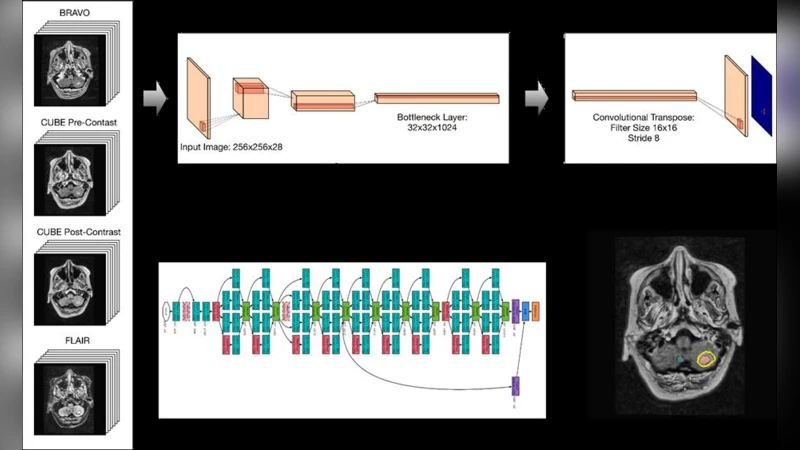
이 논문은 임상 현장에서 방사선과 의사가 다중 시퀀스 3D MRI를 해석하면서 겪는 피로도와 시간 소모를 감소시키기 위해, 딥러닝 기반 자동화 솔루션을 제안한다. 데이터는 1.5 T와 3 T 스캐너에서 획득한 네 종류의 시퀀스(전·후‑가돌리늄 T1 3D FSE, 후‑가돌리늄 T1 3D IR‑prep FSPGR, 3D FLAIR)를 포함한다. 각 환자마다 두 명의 숙련된 신경방사선과가 수작업으로 병변을 라벨링했으며, 이를 ‘ground truth’로 사용한다.
네트워크 설계는 2.5D 접근법을 채택했는데, 이는 3D 볼륨 전체를 한 번에 처리하는 대신, 인접한 3개의 연속 슬라이스를 채널 차원으로 결합해 2D CNN에 입력함으로써 메모리 효율성을 높이고, 3D 컨텍스트 정보를 유지한다. 기본 구조는 GoogLeNet(Inception) 아키텍처를 차용했으며, 초기 가중치는 ImageNet 사전학습 모델을 이용해 전이학습하였다. 마지막 레이어는 1채널 시그모이드 출력으로 바꾸어, 각 픽셀에 대한 병변 존재 확률을 제공한다.
훈련은 100명의 환자를 이용해 200 epoch까지 진행했으며, 개발 세트(5명)에서 최적 임계값을 탐색했다. 손실 함수는 Dice 손실과 바이너리 교차 엔트로피의 가중합을 사용해 클래스 불균형을 보정하였다. 데이터 증강으로는 회전, 스케일링, 강도 변형을 적용해 일반화 능력을 강화했다.
평가 지표는 ROC‑AUC, Precision, Recall, Dice/F1, 그리고 환자당 위양성(FP) 수였다. 전체 테스트군(51명)에서 AUC는 0.98로 매우 높았으며, 병변 수가 적은(1‑3개) 그룹에서 0.99, 중간(4‑10개) 및 다수(>10개) 그룹에서 각각 0.97을 기록했다. 최적 임계값(개발 세트 기반)에서는 정밀도 0.79, 재현율 0.53, Dice 0.79를 달성했으며, 이는 기존 수작업 대비 높은 정확도를 의미한다. 위양성은 평균 8.3개/환자였지만, 10 mm³ 이하 작은 병변을 제외하면 3.4개/환자로 감소한다. 이는 임상 적용 시 후처리 단계에서 크기 필터링이나 전문가 검토를 통해 충분히 관리 가능하다.
한계점으로는 데이터가 단일 기관에 국한돼 있어 외부 검증이 부족하고, MRI 시퀀스가 고정돼 있어 다른 프로토콜에 대한 일반화가 미확인이다. 또한, 2.5D 방식은 완전 3D 컨텍스트를 완전히 활용하지 못한다는 점이 있다. 향후 연구에서는 다기관 데이터셋, 다양한 스캐너·시퀀스, 그리고 3D U‑Net 같은 구조를 도입해 성능과 견고성을 높일 필요가 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기