프리온 AGAAAAGA 아밀로이드 섬유의 원자 수준 모델링을 위한 최적화 전략
안내: 본 포스트의 한글 요약 및 분석 리포트는 AI 기술을 통해 자동 생성되었습니다. 정보의 정확성을 위해 하단의 [원본 논문 뷰어] 또는 ArXiv 원문을 반드시 참조하시기 바랍니다.
초록
**
본 논문은 실험적으로 구조를 규명하기 어려운 프리온 단백질의 AGAAAAGA(113‑120) 펜타펩타이드 구간을, 기존 X‑ray·NMR 대신 수학적 최적화와 분자 동역학 시뮬레이션을 결합한 방법으로 원자 해상도의 아밀로이드 섬유 구조를 구축한다. 3NHC 템플릿을 변이시켜 3가지 모델을 만들고, 반데르발스(LJ) 상호작용을 6개의 자유도만 남겨 두고 하이브리드 이산 그래디언트·시뮬레이티드 어닐링으로 최소화한 뒤 AMBER 11로 미세조정한다. 얻어진 구조는 프리온 질환 치료제 설계에 활용 가능하다.
**
상세 분석
**
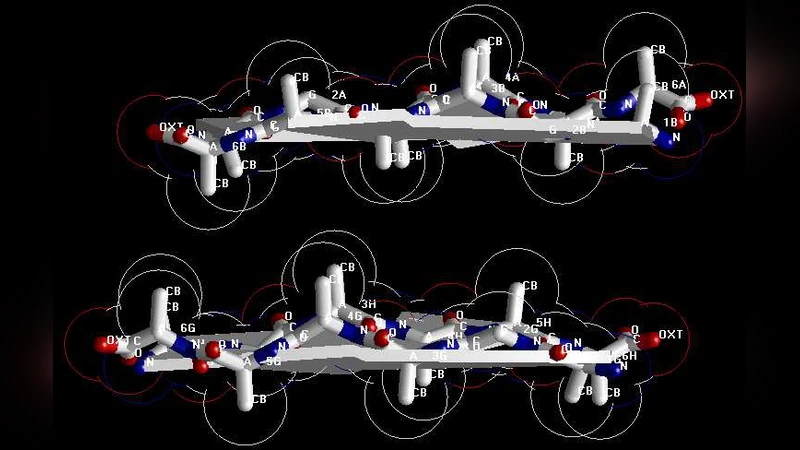
이 연구는 프리온 단백질의 핵심 병리 부위인 AGAAAAGA 펜타펩타이드가 비결정성·불용성이라 전통적인 결정학·핵자기공명(NMR)으로는 구조를 규명하기 힘든 상황을 극복하고자, 순수 계산화학적 접근을 제시한다. 먼저 인간 M129 프리온(127‑132) 펩타이드의 고해상도 스테리시스(3NHC, PDB) 구조를 템플릿으로 삼아, Swiss‑PdbViewer를 이용해 A‑B 체인을 변이시켜 세 가지 변형 모델(AAAAGA, GAAAAG, AAAAGA)을 만든다. 변이 후에도 대부분의 수소결합이 보존되므로, 주요 관심 대상은 β‑시트 사이의 반데르발스(vdw) 접촉이다.
논문은 vdw 상호작용을 Lennard‑Jones(LJ) 포텐셜 V_LJ = 4ε
댓글 및 학술 토론
Loading comments...
의견 남기기