칼슘 신호전달을 통한 시냅스 가소성 간소화 모델
초록
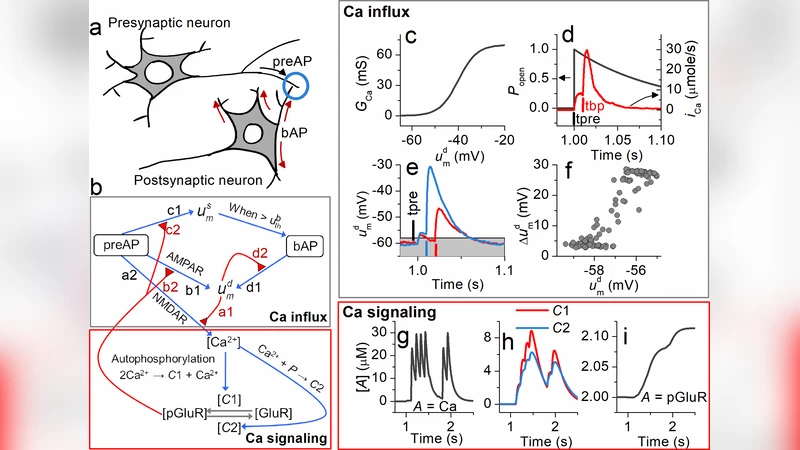
본 논문은 칼슘 유입에서 시작해 가상의 촉매 C1과 C2가 각각 글루타메이트 수용체의 인산화와 탈인산화를 매개하는 간단한 화학 반응식으로 시냅스 가소성을 모델링한다. 동기화 페어링, 전후 시냅스 전·후 전위 연계, 그리고 시각 피질의 우세도 가소성 실험을 재현하며, 역전파 활동전위(bAP)의 시냅스 특이적 강화가 경쟁 메커니즘의 핵심임을 제시한다.
상세 분석
이 연구는 기존의 칼슘 기반 시냅스 가소성 모델이 흔히 사용하는 “칼슘 농도 임계값”이라는 추상적 개념을 배제하고, 실제 화학 반응식에 기반한 구체적 메커니즘을 제시한다는 점에서 혁신적이다. 저자들은 칼슘 이온이 세포 내에 유입되면 두 종류의 가상의 촉매, C1(인산화 촉매)와 C2(탈인산화 촉매)를 각각 활성화한다는 가정을 도입한다. C1은 Ca²⁺와 결합해 AMPA 수용체의 인산화를 촉진함으로써 장기 강화(LTP)를, C2는 Ca²⁺와 결합해 동일 수용체의 탈인산화를 촉진해 장기 억제(LTD)를 유도한다. 이러한 반응은 Michaelis‑Menten 형태의 속도식으로 기술되어, 칼슘 농도와 촉매 활성도의 비선형 관계를 정량적으로 설명한다.
모델 검증을 위해 두 가지 전형적인 실험 프로토콜을 적용하였다. 첫 번째는 전시냅스와 후시냅스 전위가 정확히 동기화되는 페어링 프로토콜이며, 두 번째는 전시냅스와 후시냅스 전위가 일정 시간 차이를 두고 발생하는 시차 의존성 프로토콜이다. 두 경우 모두 시뮬레이션 결과가 실제 전기생리학적 데이터와 일치했으며, 특히 C1과 C2의 활성 비율이 시간 차이에 따라 어떻게 전환되는지가 명확히 드러났다.
또한, 저자들은 두 개의 시냅스가 동일한 뉴런에 연결된 상황에서 역전파 활동전위(bAP)의 강도가 시냅스마다 다르게 조절될 수 있음을 가정한다. bAP는 후전위가 역방향으로 전파될 때 발생하는 전위이며, 이는 각 시냅스의 칼슘 유입량을 차등적으로 증가시킨다. 결과적으로, bAP가 강하게 전달되는 시냅스는 C1이 우세하게 활성화되어 LTP를, 약하게 전달되는 시냅스는 C2가 우세해 LTD를 겪는다. 이러한 메커니즘은 Bienenstock‑Cooper‑Munro(BCM) 이론에서 제시된 “활동 의존적 가소성 임계값”을 물리적·화학적 과정으로 구체화한다는 점에서 의미가 크다.
모델의 강점은 (1) 화학 반응식 기반으로 파라미터 추정이 가능하고, (2) 다양한 실험 프로토콜을 통합적으로 설명할 수 있으며, (3) 시냅스 간 경쟁을 bAP라는 실제 생리학적 현상에 귀속시켜 BCM 이론을 실증적으로 재구성한다는 점이다. 반면, C1·C2와 같은 가상의 촉매가 실제 세포 내 어떤 단백질에 해당하는지에 대한 실험적 검증이 부족하고, 모델이 단일 뉴런 수준에 국한돼 네트워크 수준의 확장 가능성에 대한 논의가 미흡하다는 한계도 존재한다.
댓글 및 학술 토론
Loading comments...
의견 남기기