혈관을 좌표계로 활용한 인간 세포 지도 구축 방안
초록
본 논문은 인간 전체 세포를 3차원 좌표계에 배치하기 위한 공통 좌표 프레임워크(CCF)로서 혈관망을 활용하는 가능성을 검토한다. 현재 진행 중인 Human Cell Atlas, Human Protein Atlas, HuBMAP 등 다중 프로젝트가 다양한 인구집단의 조직 샘플을 수집하고 있으나, 이들을 통합해 일관된 공간적 ‘주소’를 부여하려면 표준화된 기준이 필요하다. 혈관은 전신에 걸쳐 연속적이고 계층적인 구조를 가지고 있어, 장기 수준부터 미세 조직 단위, 개별 세포까지 일관된 기준점을 제공한다. 논문은 혈관 기반 CCF의 장점(보편성, 정량적 측정 가능성, 기능적 연관성)과 구현 시 고려해야 할 기술적·생물학적 도전 과제(이미징 해상도, 변이성, 동적 변화) 등을 제시한다.
상세 분석
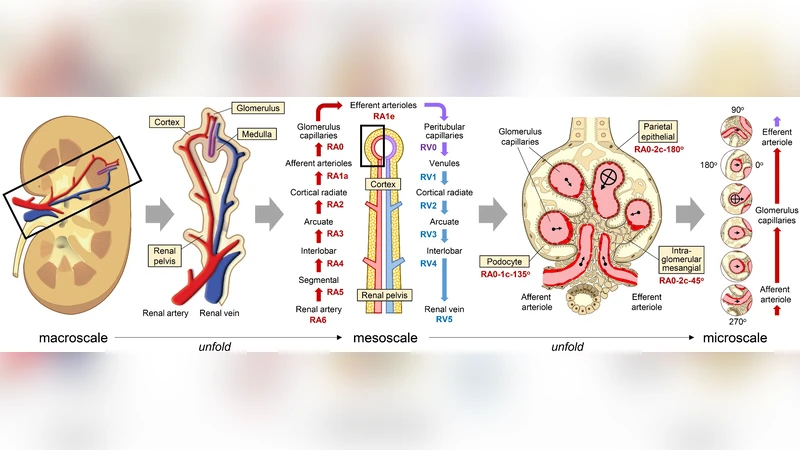
이 논문은 인간 전체 세포 지도 구축을 위한 좌표 체계 선택 문제를 ‘혈관 기반 공통 좌표 프레임워크(CCF)’라는 새로운 관점으로 접근한다. 기존 CCF 후보로는 해부학적 랜드마크, 조직 경계, 유전적 마커 등이 제시돼 왔지만, 전신 규모에서 일관된 정밀도를 유지하기는 어려웠다. 혈관은 발생학적으로 최초 형성된 원시관이 체계적으로 분지·합류하며 전신을 관통하는 네트워크를 이루므로, ‘좌표축’ 역할을 자연스럽게 수행한다. 특히 대동맥에서 미세 모세혈관까지 연속성을 갖는 구조는 다중 스케일(기관·피라미드·세포) 정렬을 가능하게 한다.
논문은 혈관 기반 CCF의 주요 장점을 세 가지로 구분한다. 첫째, 보편성이다. 모든 인간은 기본적인 혈관 패턴을 공유하므로, 인종·연령·성별에 따른 변이가 있더라도 핵심 골격은 유지된다. 둘째, 정량적 측정 가능성이다. 혈관은 혈류 속도, 직경, 분지 각도 등 물리적 파라미터를 정밀하게 측정할 수 있는 대상이며, MRI, CT, 광학 클리어링 등 다양한 영상기법으로 3D 형태를 고해상도로 재구성할 수 있다. 셋째, 기능적 연관성이다. 세포는 혈관 근처에서 영양·산소·신호를 공급받으며, 면역세포·줄기세포·대사세포 등은 혈관을 따라 이동한다. 따라서 좌표를 혈관에 매핑하면 세포 간 상호작용과 미세환경을 동시에 파악할 수 있다.
하지만 구현 단계에서는 여러 도전 과제가 존재한다. 첫째, 영상 해상도와 스케일 격차이다. 전신 MRI는 수밀리미터 수준이지만, 세포 수준에서는 나노미터 정밀도가 필요하다. 멀티모달 데이터 통합을 위한 정합 알고리즘 개발이 필수적이다. 둘째, 혈관 변이성이다. 개인마다 혈관 길이·분지 패턴이 미세하게 다르며, 질병(동맥경화, 종양 혈관신생)이나 생활 습관에 따라 구조가 변한다. 이러한 변이를 모델링하고 보정하는 표준화 절차가 필요하다. 셋째, 동적 변화이다. 혈관은 발달, 성장, 노화 과정에서 구조적 재구성을 겪으며, 심박동·혈류 변화도 실시간으로 좌표를 움직이게 만든다. 정적 CCF와 동적 CCF를 어떻게 조화시킬지에 대한 전략이 요구된다.
기술적 측면에서는 광학 클리어링·라이트시트 현미경을 이용한 전신 투명화와 고해상도 스캔, 멀티플렉스 시퀀싱을 통한 혈관 내피세포와 주변 조직의 전사체 매핑, 그리고 인공지능 기반 이미지 정합이 핵심 도구로 제시된다. 또한, 혈관을 기준으로 한 좌표 변환 매트릭스를 정의하고, 이를 국제 표준 파일 포맷(예: OME‑XML)과 연동함으로써 다양한 연구기관 간 데이터 교환을 원활히 할 수 있다.
결론적으로, 혈관을 CCF의 골격으로 삼는 접근은 해부학적 일관성, 측정 가능성, 기능적 연관성이라는 세 축을 동시에 만족시킨다. 다만, 고해상도 영상 획득, 개인 변이 보정, 동적 모델링 등 기술·생물학적 난제를 해결하기 위한 다학제 협력이 필수적이다. 향후 이러한 혈관 기반 CCF가 성공적으로 구현된다면, 인간 세포 지도는 단순히 정적인 위치 정보가 아니라, 혈류·대사·면역 네트워크와 결합된 ‘생물학적 지도’로 진화할 전망이다.
댓글 및 학술 토론
Loading comments...
의견 남기기