발달을 이끄는 숨은 힘, 기저측액의 수분 조절
초록
본 리뷰는 배아 발달 과정에서 세포 외액, 특히 기저측(fluid) 공간의 수분 함량과 물리·화학적 특성이 조직 형성에 미치는 역할을 조명한다. 마우스와 제브라피시 초기 배아를 모델로 삼아, 조직 수분이 시공간적으로 어떻게 조절되고, 이 조절이 세포 이동, 형태 변형, 장기 배치 등에 어떤 영향을 주는지를 최신 연구들을 종합적으로 정리한다.
상세 분석
이 논문은 전통적으로 세포 자체의 기계적 특성(예: 세포 수축, 접착, 골격 재배열)만을 발달의 구동기로 여겨온 관점을 탈피한다. 저자들은 배아 조직이 ‘액체 매트릭스’에 잠겨 있다는 점에 주목하며, 특히 기저측액(basolateral fluid)이 세포와 세포 사이, 그리고 세포와 기저막 사이에 형성하는 미세한 수분 환경을 핵심 엔진으로 제시한다. 첫 번째 핵심 인사이트는 ‘수분 압력’이다. 배아 내외부의 삼투압 차이가 조직 팽창을 유도하고, 이는 세포 간 거리와 세포 외 기질의 물리적 강성을 동시에 변화시켜 세포 이동 경로와 형태 변화를 조절한다. 두 번째는 ‘이온 및 용질 농도 구배’이다. Na⁺, K⁺, Ca²⁺와 같은 이온이 기저측액에 비대칭적으로 분포하면 전기화학적 구배가 형성돼, 세포 내 신호전달(예: Ca²⁺ 스파이크)과 세포 골격 재조직을 유도한다. 세 번째는 ‘액체 흐름과 전단력’이다. 초기에 형성되는 체강(예: 원시 심낭, 신경관) 내부의 액체 흐름은 전단력을 발생시켜, 세포가 특정 방향으로 정렬하거나, 기저막을 따라 이동하도록 한다. 네 번째는 ‘수분 조절 메커니즘의 유전적·분자적 기반’이다. Aquaporin(특히 AQP1, AQP3) 발현 조절, Na⁺/K⁺-ATPase 및 클라트린 매개 수송체의 활성화가 조직 수분 함량을 시공간적으로 미세조정한다는 증거가 제시된다.
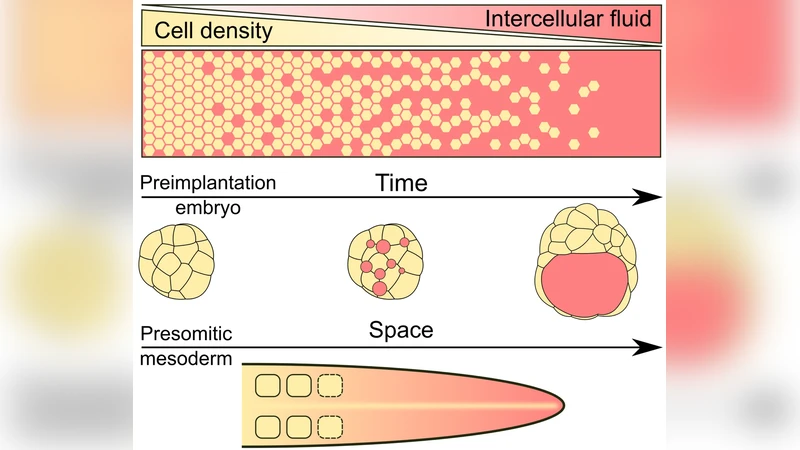
마우스 배아에서는 착상 후 3.5일경부터 자궁강 내 액체가 급격히 증가하고, 이는 배아 외피(TE)와 기저막 사이에 고압의 기저측액을 형성한다. 이 압력은 TE 세포의 확장과 분열을 촉진하고, 동시에 원시 원시엽(epiblast)의 내부 압축을 유도해 원시 신경관 형성에 기여한다. 제브라피시에서는 투명한 외부 막을 통해 물이 빠르게 유입되면서, 배아 전체가 ‘수분 팽창 단계’를 겪는다. 이 단계에서 발생하는 전신적인 수분 증가가 체축 길이와 체세포 간 거리 확대를 일으키며, 이는 후속 형태 형성(예: 몸통 길이, 꼬리 형성)과 직접 연결된다.
또한, 저자들은 실험적 접근법으로 마이크로인젝션, 광학적 트래핑, 그리고 고해상도 라만 스펙트로스코피를 활용해 기저측액의 조성 변화를 실시간으로 측정하고, 이를 유전적 교란(예: AQP 결손, Na⁺/K⁺-ATPase 억제)과 연계시켜 기능적 인과관계를 규명한 사례들을 정리한다. 이러한 방법론은 기존의 조직학적 관찰을 넘어, ‘액체 역학’이라는 새로운 차원의 발달 연구를 가능하게 한다.
결과적으로, 기저측액은 단순히 세포를 둘러싼 ‘배경’이 아니라, 수분 함량, 이온 구배, 전단력, 그리고 유전적 조절 메커니즘을 통해 조직 형태와 기능을 직접적으로 ‘설계’하는 핵심 요소임이 강조된다. 이는 향후 재생 의학, 장기 오가노이드 제작, 그리고 선천성 기형 예방 전략에 물리·화학적 환경을 정밀하게 제어하는 새로운 패러다임을 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기