프로스테이트 CT 방사선 치료를 위한 적대적 최적화 기반 공동 정합 및 분할
안내: 본 포스트의 한글 요약 및 분석 리포트는 AI 기술을 통해 자동 생성되었습니다. 정보의 정확성을 위해 하단의 [원본 논문 뷰어] 또는 ArXiv 원문을 반드시 참조하시기 바랍니다.
초록
본 연구는 고정 영상과 이동 영상, 그리고 두 영상의 라벨을 학습 단계에서만 이용하고 테스트 단계에서는 라벨 없이도 3차원 변형 벡터 필드(DVF)를 추정하는 적대적 신경망을 제안한다. 생성기(Generator)는 DVF를 예측하고, 판별기(Discriminator)는 정합된 영상과 라벨의 일치를 평가한다. 프로스테이트 CT 데이터셋에 적용한 결과, 전통적인 elastix 기반 정합보다 평균 표면 거리와 95% Hausdorhaus 거리 모두에서 유의하게 개선되었으며, 실행 시간은 0.6초로 실시간 적용이 가능함을 보였다.
상세 분석
이 논문은 의료 영상 분야에서 오래된 과제인 이미지 정합(registration)과 세그멘테이션(segmentation)을 하나의 딥러닝 프레임워크로 통합하려는 시도이다. 핵심 아이디어는 적대적 학습(Generative Adversarial Network, GAN)을 이용해 정합 품질을 직접 판별기에 피드백함으로써, 전통적인 두 단계(open‑loop) 방식의 한계를 극복하는 것이다.
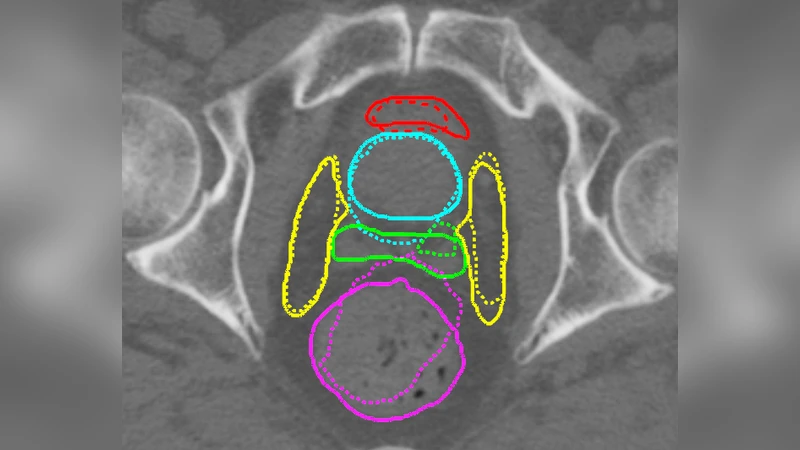
- 학습 설정: 고정 영상(I_f)과 이동 영상(I_m)뿐 아니라 두 영상에 대한 라벨(S_f, S_m)도 학습 단계에서 제공한다. 테스트 단계에서는 라벨이 필요 없으며, 이는 방사선 치료에서 매일 촬영되는 CT에 대해 실시간으로 컨투어를 전파해야 하는 실제 임상 상황에 부합한다.
- 생성기 구조: 3D U‑Net 형태의 인코더‑디코더 네트워크를 사용해 I_f와 I_m을 입력으로 받아 변형 벡터 필드 Φ를 출력한다. 출력 크기를 입력보다 작게 설계해 넓은 수용 영역을 확보하고, NiftyNet의 리샘플링 모듈을 통해 Φ에 의해 변형된 이미지와 라벨을 즉시 생성한다. 이는 엔드‑투‑엔드 학습을 가능하게 한다.
- 판별기 설계: PatchGAN을 차용해 입력을 (I_f, I_m(Φ), S_m(Φ)) 형태의 3채널 텐서로 구성한다. 두 가지 변형을 실험했는데, 하나는 라벨을 별도 채널로 입력하고(JRS‑GAN a), 다른 하나는 라벨을 이미지와 곱해 구조적 강조를 유도한다(JRS‑GAN b). 판별기는 지역적인 정합 품질을 스칼라가 아닌 패치 단위로 평가함으로써 미세한 변형 오류도 감지한다.
- 손실 함수: 기본 GAN 손실은 Wasserstein GAN(WGAN) 형태로 안정성을 확보한다. 그러나 WGAN만으로는 수렴이 느리고 정합 정확도가 떨어져, 추가적인 유사도 손실 L_sim을 도입했다. L_sim은 (1‑DSC)와 (1‑NCC) 두 항을 포함해 라벨 겹침과 이미지 강도 정합을 동시에 최적화한다. 또한, 변형 필드의 매끄러움을 보장하기 위해 L_smooth(벡터 필드의 베딩 에너지)와 λ₁, λ₂ 가중치를 사용한다.
- 학습 전략: 초기 25 epoch 동안 생성기 1회당 판별기 100회를 학습해 판별기의 판별 능력을 빠르게 강화하고, 이후 1:5 비율로 전환한다. 판별기 파라미터는 WGAN 요구에 따라 클리핑을 적용한다.
- 데이터 및 평가: 18명의 전립선 암 환자(각 7~10회 반복 CT)에서 111개의 학습/검증 쌍과 50개의 테스트 쌍을 구성했다. 평가 지표는 평균 표면 거리(MSD)와 95% Hausdorff 거리(HD)이며, 통계적 유의성 검증을 위해 Wilcoxon signed‑rank test(p = 0.05)를 사용했다.
- 실험 결과: 모든 비교군(elastix‑NCC, elastix‑MI, Reg‑CNN, JRS‑CNN, Reg‑GAN)보다 JRS‑GAN a/b가 MSD와 HD 모두에서 유의하게 낮은 값을 기록했다. 특히 방광·직장 등 위험 기관의 HD 감소가 두드러졌다. Jacobian determinant의 표준편차는 elastix‑MI(0.08)보다 JRS‑GAN a(0.17)에서 더 큰 변형 다양성을 보였지만, 이는 정합 정확도 향상과 상충되지 않는다. 실행 시간은 GPU(V100) 기준 0.6 초로, CPU 기반 elastix(13 초) 대비 20배 이상 빠르다.
핵심 인사이트: (1) 라벨 정보를 정합 과정에 직접 활용하면 정합 정확도가 크게 향상된다. (2) 적대적 피드백은 단순한 정합 손실만 사용할 때보다 미세한 구조적 정합을 학습하는 데 도움이 된다. (3) 3D GAN을 이용한 엔드‑투‑엔드 학습은 실시간 방사선 치료 워크플로우에 적합한 속도와 정확성을 동시에 제공한다. 향후 연구에서는 Gradient‑Penalty 기반 WGAN, 다중‑스케일 판별기, 그리고 다른 장기(예: 간, 폐)로의 일반화 검증이 기대된다.
댓글 및 학술 토론
Loading comments...
의견 남기기