유연한 암 연관 크로마틴 구성은 암 치료 난이도의 근본 원인
초록
본 논문은 세포 유형을 결정하는 염색질 구성이 암에서도 적용된다고 가정하고, 암 특유의 유연한 크로마틴 구조(CACC)가 세포의 전능성 및 환경 적응을 촉진해 이질적인 종양 하위클론을 생성하고, DNA 복제·전사·복구·돌연변이 등 핵심 유전체 활동을 효율적으로 이용하게 만든다고 주장한다. 따라서 CACC의 유연성을 제한하거나 정상형으로 전환시키는 전략이 암 치료의 새로운 방향이 될 수 있다.
상세 분석
이 논문은 기존의 암 발생 모델이 주로 유전적 변이와 신호 전달 경로의 이상에 초점을 맞춘 반면, 염색질 수준의 구조적 유연성이 종양의 적응성과 이질성을 근본적으로 좌우한다는 가설을 제시한다. 저자들은 ‘세포 유형 연관 염색질 구성(cell‑type‑associated chromatin configuration, CTACC)’이라는 개념을 도입해, 정상 세포가 특정 발달 단계와 조직 특성을 유지하는 데 필요한 고정된 염색질 패턴을 가지고 있다고 설명한다. 반면, 암세포는 ‘암 연관 크로마틴 구성(CACC)’이라는 보다 가변적인 염색질 상태를 띠며, 이는 히스톤 변형, DNA 메틸화, 고차원 루프 구조 등 다중 레이어에서 동적으로 재조정된다.
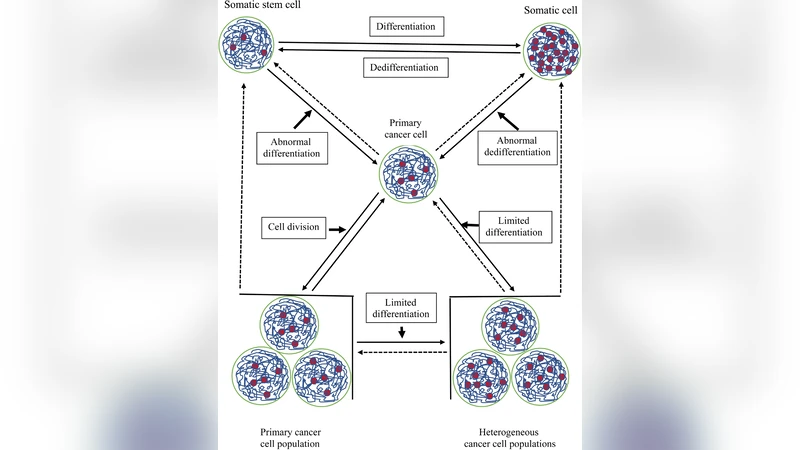
핵심적인 통찰은 CACC의 ‘유연성’이 세 가지 측면에서 암의 치료 저항성을 강화한다는 점이다. 첫째, 유연한 염색질은 전사 인자와 복제 기계가 다양한 유전자 좌표에 접근하도록 허용해, 필요에 따라 특정 유전자를 활성화하거나 억제함으로써 세포 생존에 최적화된 전사·복제 프로그램을 즉시 재구성한다. 둘째, 이러한 구조적 변동성은 DNA 손상 복구 경로를 선택적으로 전환시켜, 급격한 스트레스(예: 방사선, 화학요법) 상황에서도 손상된 DNA를 효율적으로 복구하거나, 오히려 돌연변이 발생을 촉진해 새로운 적응형 변이를 생성한다. 셋째, CACC는 ‘제한된 분화’를 통해 이질적인 종양 하위클론을 지속적으로 생산한다. 즉, 완전한 다능성으로 되돌아가는 것이 아니라, 특정 전구체 상태에 머무르면서도 다양한 전사적·표현형적 변이를 동시에 발현한다는 점이다.
저자들은 이러한 메커니즘을 뒷받침하기 위해 기존의 ATAC‑seq, Hi‑C, ChIP‑seq 데이터들을 재해석하고, 암세포주와 정상 조직 간의 염색질 접근성 차이를 정량화한다. 결과는 암세포가 정상 세포에 비해 전반적인 염색질 개방도가 높으며, 특히 전사 억제 영역과 복제 기점 사이의 경계가 흐려지는 현상을 보인다. 이는 ‘유연한 CACC’가 전사·복제·복구 네트워크를 통합적으로 재배열함을 시사한다.
마지막으로, 논문은 치료 전략으로 두 가지 접근을 제안한다. (1) CACC의 유연성을 물리적으로 제한하는 약물(예: 히스톤 탈아세틸화 효소 활성제, DNA 메틸화 강화제) 개발, (2) CACC를 정상형 CTACC로 ‘재프로그래밍’하는 전사인자 재조합 혹은 CRISPR‑based 에피제네틱 편집 기술이다. 이러한 전략은 암세포를 ‘정상화’시키거나, 최소한 악성도를 감소시켜 기존 치료와 시너지 효과를 낼 가능성을 제시한다.
전반적으로 이 논문은 암 연구에 새로운 차원의 구조적·에피제네틱 관점을 도입함으로써, 기존의 유전적·신호전달 중심 모델을 보완하고, 치료 저항성의 근본 원인을 설명하려는 시도를 보여준다.
댓글 및 학술 토론
Loading comments...
의견 남기기