ADAM30이 알츠하이머에서 APP 결함을 억제한다
초록
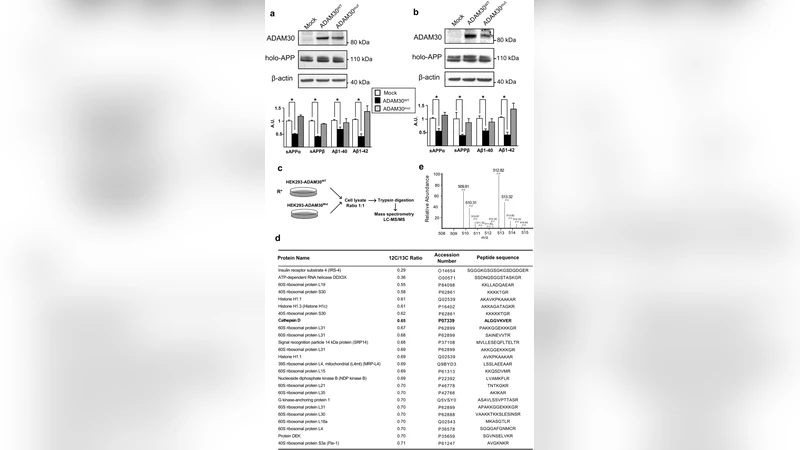
본 연구는 ADAM30의 발현이 알츠하이머 병변에서 감소하고, ADAM30이 APP를 리소좀으로 이동시켜 카텝신 D를 활성화함으로써 Aβ 생성과 축적을 억제한다는 것을 보여준다. ADAM30을 과발현하면 Aβ42 분비와 뇌 내 플라크가 감소하고, 시냅스 가소성인 LTP가 회복된다.
상세 분석
이 논문은 ADAM30이 알츠하이머 병리에서 수행하는 새로운 기능을 다각도로 입증한다. 첫째, 인간 알츠하이머 뇌 조직의 전사체 데이터를 분석한 결과, ADAM30 mRNA가 정상 대조군에 비해 약 50% 감소했으며, 이 감소 정도는 뇌 내 아밀로이드 플라크 양과 역상관 관계를 보였다. 이는 ADAM30이 질병 진행에 억제적 역할을 할 가능성을 시사한다. 둘째, SH‑SY5Y와 HEK293 세포에서 ADAM30을 siRNA로 억제하거나 lentiviral 벡터로 과발현함으로써 Aβ40·Aβ42 농도를 각각 상승·감소시켰다. 특히 촉매 도메인이 비활성화된 돌연변이형 ADAM30(mut)은 Aβ 수준에 영향을 주지 않아, 효소 활성이 핵심 메커니즘임을 확인했다. 셋째, 질량분석 기반 프로테오믹스와 면역침전 실험을 통해 ADAM30이 카텝신 D(CTSD) 전구체를 직접 절단해 활성 형태로 전환한다는 사실을 밝혀냈다. 활성화된 CTSD는 리소좀 내에서 APP를 분해하거나 리소좀으로의 재분류를 촉진한다는 것이 추가 실험으로 입증되었다. 네번째, ADAM30 과발현 마우스 모델(Thy1‑ADAM30)에서 신경세포 특이적 발현이 확인되었으며, 이 마우스의 1차 신경세포 배양액에서 Aβ42 분비가 현저히 감소했다. 동일 마우스의 뇌 조직에서는 용해성 Aβ42와 전반적인 플라크 부피가 현저히 낮아졌고, CTSD 활성이 상승했다. 마지막으로, 전기생리학적 기록을 통해 ADAM30 과발현 마우스는 장기 강화(LTP) 결함이 회복되었으며, 이는 시냅스 기능 회복과 직접 연관될 수 있음을 시사한다. 전체적으로 ADAM30‑CTSD 축은 APP 대사를 리소좀 경로로 전환시켜 병리적 Aβ 축적을 억제하는 새로운 치료 표적으로 부각된다.
댓글 및 학술 토론
Loading comments...
의견 남기기