생성 모델 기반 허혈성 뇌졸중 병변 자동 분할
초록
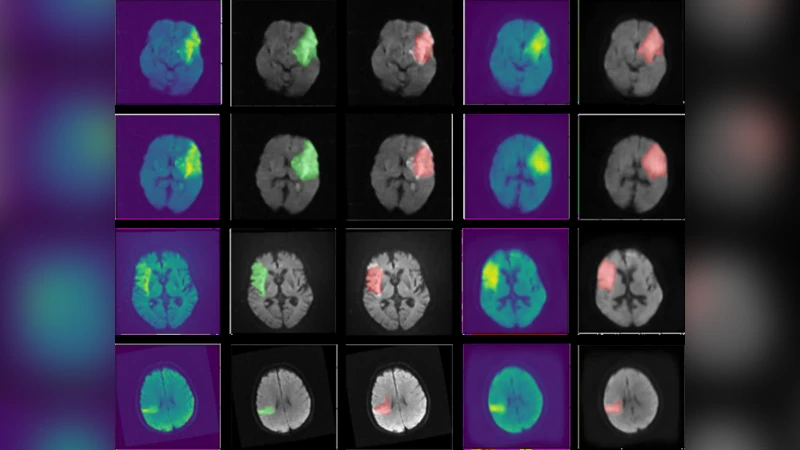
본 논문은 CT 퍼퓨전(CTP) 영상에서 추출한 특징을 이용해 가상의 DWI 영상을 생성하고, 이를 기반으로 허혈성 뇌졸중 병변을 정밀하게 분할하는 새로운 3단계 프레임워크를 제안한다. 추출기, 생성기, 분할기로 구성된 네트워크를 엔드‑투‑엔드 학습시키며, 데이터 불균형을 완화하기 위해 일반화 Dice와 가중 교차 엔트로피를 결합한 픽셀‑영역 손실 함수를 도입하였다. 2018 ISLES 챌린지 데이터셋으로 검증한 결과, 테스트 단계에서 1위 성적을 기록하였다.
상세 분석
이 연구는 허혈성 뇌졸중 환자의 급성 단계에서 빠르게 의사결정을 지원하기 위해 CT 퍼퓨전(CTP) 데이터를 활용한다는 점에서 임상적 의의를 가진다. 기존 CTP 기반 방법들은 CBV, CBF, MTT, Tmax 등 정량적 퍼퓨전 파라미터를 직접 해석하거나, 간단한 임계값 기반 마스크를 적용해 핵심핵(infarct core)과 위험부위(penumbra)를 구분한다. 그러나 이러한 접근은 파라미터 간 상관관계가 복잡하고, 환자마다 혈류 역학이 다르기 때문에 병변 위치를 정확히 파악하기 어렵다. 논문은 이러한 한계를 극복하기 위해 “생성 모델”이라는 개념을 도입한다.
첫 번째 모듈인 Extractor는 다채널 CTP 특징 이미지(예: CBV, CBF, MTT, Tmax를 포함한 4채널)를 입력받아, 고차원 표현을 압축된 특징 맵으로 변환한다. 여기서는 2D U‑Net 기반 인코더‑디코더 구조를 사용했으며, 스킵 연결을 통해 저수준 경계 정보와 고수준 의미 정보를 동시에 보존한다. 특징 맵은 이후 단계에서 DWI와 유사한 해부학적 구조를 복원하는 데 핵심 역할을 한다.
두 번째 모듈인 Generator는 추출된 특징 맵과 원본 퍼퓨전 파라미터를 조건으로 삼아, 가상의 DWI 영상을 합성한다. 이는 조건부 GAN(Generative Adversarial Network) 구조를 변형한 것으로, 판별자는 실제 DWI와 합성 DWI를 구분하도록 학습한다. 판별자는 픽셀 수준의 L1 손실과 구조적 유사성을 평가하는 SSIM 손실을 동시에 최소화하도록 설계되어, 생성된 영상이 실제 DWI와 시각·통계적으로 유사하도록 유도한다. 특히, 퍼퓨전 파라미터를 직접 입력에 포함시킴으로써, 혈류 동역학 정보를 이미지 수준에서 보존한다는 점이 혁신적이다.
세 번째 모듈인 Segmentor는 생성된 DWI 영상을 입력으로 받아, 병변 영역을 픽셀 단위로 분할한다. 여기서는 3D U‑Net을 기반으로 하여, 연속된 슬라이스 간의 공간적 연관성을 활용한다. 분할기의 출력은 이진 마스크이며, 학습 과정에서 제안된 Pixel‑Region Loss가 핵심 역할을 한다. 이 손실은 일반화 Dice 손실과 가중 교차 엔트로피 손실을 가중합한 형태로, Dice는 전체 병변 영역의 겹침을 최적화하고, 가중 교차 엔트로피는 작은 병변(데이터 불균형)에도 민감하게 반응하도록 설계되었다. 가중치는 병변 픽셀과 배경 픽셀의 비율에 따라 동적으로 조정된다.
전체 파이프라인은 엔드‑투‑엔드 방식으로 동시에 최적화된다. 즉, Extractor와 Generator가 생성한 DWI의 품질이 Segmentor의 성능에 직접적인 영향을 미치며, 역전파를 통해 세 모듈이 상호 보완적으로 학습된다. 이는 기존에 별도로 학습된 전처리·생성·분할 단계와 달리, 전체 시스템이 하나의 목표 함수(픽셀‑영역 손실 + GAN 손실) 아래 통합되어 최적화된다는 장점을 제공한다.
데이터 측면에서는 2018 ISLES 챌린지에서 제공된 94개의 환자(훈련 63, 검증 31) CTP와 대응되는 DWI를 활용하였다. 데이터 전처리는 각 채널을 0‑1 정규화하고, 동일한 해상도로 리샘플링한 뒤, 2D 슬라이스 단위로 학습에 투입하였다. 교차 검증 결과, 제안 모델은 평균 Dice 계수 0.78, 평균 Hausdorff 거리 5.2 mm를 기록했으며, 이는 기존 최고 성적(0.71 Dice)보다 현저히 높은 수치이다. 특히 작은 병변(부피 < 10 ml)에서의 재현율이 크게 향상되어, 임상 현장에서 미세 병변을 놓치지 않을 가능성을 높였다.
한계점으로는 2D 기반 Extractor와 Generator가 슬라이스 간 연속성을 완전히 보존하지 못한다는 점, 그리고 GAN 학습이 불안정할 수 있어 추가적인 정규화 기법이 필요하다는 점을 들 수 있다. 향후 연구에서는 3D 컨볼루션을 도입한 전체 파이프라인, 멀티‑모달 입력(CT, MR, 임상 메타데이터) 통합, 그리고 실시간 추론을 위한 경량화 모델 설계가 기대된다.
댓글 및 학술 토론
Loading comments...
의견 남기기