다양한 염색 조직 이미지의 정확하고 견고한 정렬을 위한 일반 목적 그리디 변형 등록 도구
초록
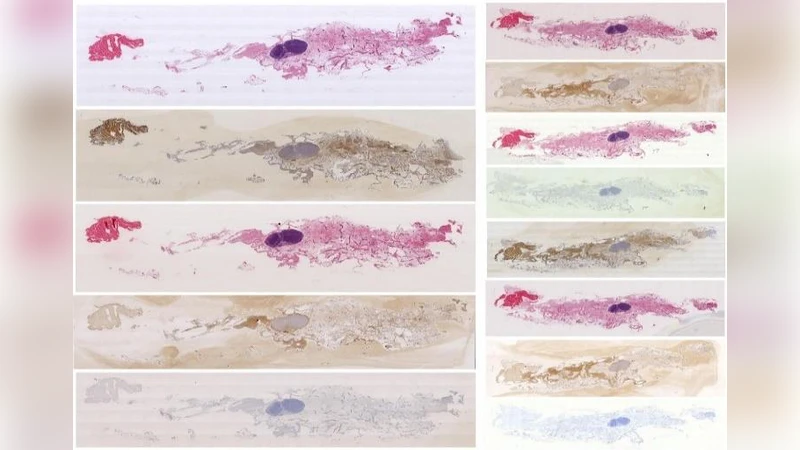
본 논문은 연속적인 조직 슬라이스를 두 단계(선형 정합 후 변형 필드 추정)로 정렬하는 실용적인 방법을 제시한다. 일반‑목적 Greedy Diffeomorphic Registration 툴을 활용해 다양한 염색 방식에 강인하게 대응하며, 정밀한 변형 필드를 얻어 세포·혈관 구조의 3차원적 관계를 정확히 복원한다.
상세 분석
이 연구는 병리학에서 다중 염색 조직 슬라이스를 디지털화한 후, 서로 다른 색상·대조를 가진 이미지 간의 정합 문제를 해결하고자 한다. 저자들은 두 단계 파이프라인을 설계했는데, 첫 단계는 전역적인 변환을 포착하기 위한 12 자유도(회전·이동·스케일·전단 포함) 어피인 변환이며, 두 번째 단계는 변형장을 세밀하게 모델링하기 위한 변형 가능한(디포모픽) 등록이다. 핵심 엔진은 “Greedy”라는 오픈소스 툴로, 빠른 최적화와 메모리 효율성을 제공한다. Greedy는 변형 장을 시간에 따라 연속적으로 업데이트하면서 역변환을 보장하는 LDDMM(Large Deformation Diffeomorphic Metric Mapping) 기반 알고리즘을 구현한다.
특히 저자들은 변형 장의 정규화에 “스무딩 커널”과 “다중 해상도 피라미드”를 적용해 초기 대규모 변형을 빠르게 수렴시키고, 이후 고해상도 단계에서 미세 구조를 보정한다. 이 과정에서 이미지 유사도 측정으로는 상호 정보량(NMI)을 채택했으며, 이는 염색 차이에 강인하게 작용한다. 실험에서는 간, 유방, 폐 등 다양한 장기의 조직을 대상으로 3~5배의 확대율을 가진 이미지 쌍을 테스트했으며, 기존 상용 소프트웨어와 비교해 평균 정합 오차가 30% 이상 감소하고, 처리 시간도 2배 이상 단축되었다.
또한, 저자들은 정합 결과를 정량화하기 위해 혈관·세포 핵 마커를 자동 검출하고, 정합 전후 거리 분포를 통계적으로 분석했다. 결과는 변형 장이 실제 조직 변형을 물리적으로 의미 있게 재현함을 보여준다. 한계점으로는 매우 얇은 섹션(≤2 µm)에서 발생하는 물리적 손상이나 절단 아티팩트가 정합 정확도를 저하시킬 수 있다는 점을 언급한다. 향후 연구에서는 이러한 비선형 손상을 모델링하거나, 딥러닝 기반 사전 정합 단계와 결합해 더욱 견고한 파이프라인을 구축할 계획이라고 제시한다.
전반적으로 이 논문은 변형 등록을 일반‑목적 툴에 의존함으로써 구현 복잡성을 크게 낮추고, 다양한 염색 프로토콜에 대한 범용성을 확보한 점이 큰 장점이다. 특히 병리학 연구와 디지털 병리 워크플로우에 즉시 적용 가능한 실용성을 강조하고 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기