MITK ModelFit: 의료 영상 모델 피팅을 위한 범용 오픈소스 프레임워크
초록
본 논문은 의료 영상 데이터에 대한 모델 피팅을 일반화하고 확장성을 제공하는 MITK-ModelFit 프레임워크를 소개한다. 로컬 모델, 피팅 인프라스트럭처, 결과 표현을 추상화하여 이미지 모달리티와 모델 종류에 구애받지 않고 적용할 수 있다. MITK와의 긴밀한 통합을 통해 데이터 로딩·전처리·후처리와 자연스럽게 연결되며, DCE‑MRI를 예시로 한 플러그인 세트를 제공한다. 디지털 팬텀 실험에서 기존 방법과 비교해 경쟁력 있는 정확도를 보였으며, 개발자와 최종 사용자를 모두 만족시키는 유연하고 검증된 도구를 목표로 한다.
상세 분석
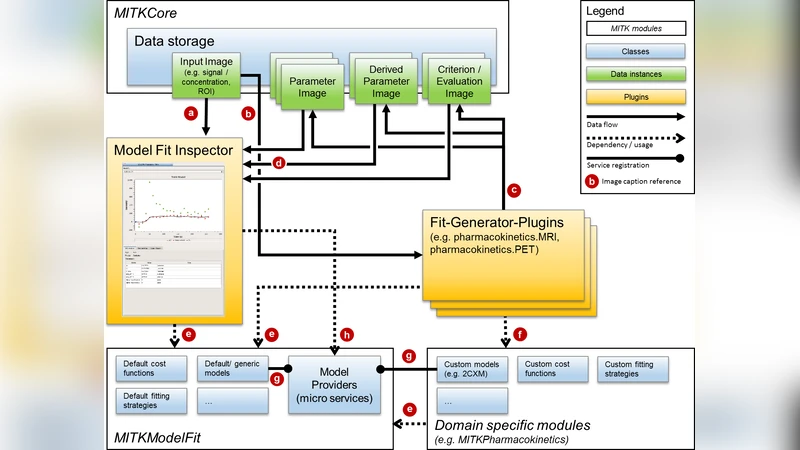
MITK‑ModelFit은 모델 피팅 작업을 의료 영상 워크플로우에 원활히 삽입하기 위해 설계된 모듈형 프레임워크이다. 핵심 설계는 세 가지 추상 계층으로 나뉜다. 첫째, LocalModel 인터페이스는 파라미터 수, 초기값, 경계, 비용 함수 등을 정의하며, 사용자는 새로운 물리·생물학적 모델을 이 인터페이스를 구현함으로써 손쉽게 추가할 수 있다. 둘째, FitEngine은 선택된 모델과 이미지 데이터(다중 채널, 시계열 등)를 받아 최적화 알고리즘(Levenberg‑Marquardt, Trust‑Region 등)을 적용한다. 엔진은 멀티스레딩과 GPU 가속을 선택적으로 활용하도록 설계돼 대용량 4D 데이터에서도 실시간 피팅이 가능하도록 한다. 셋째, FitResult 객체는 파라미터 맵, 잔차 이미지, 피팅 품질 지표(R², AIC 등)를 포함하며, MITK의 데이터 노드 구조에 그대로 매핑된다. 이러한 추상화는 모델, 최적화 기법, 결과 시각화를 독립적으로 교체·확장할 수 있게 하여, 기존 DCE‑MRI, DW‑MRI, CEST 등 다양한 분야에 재사용성을 제공한다.
프레임워크는 MITK 플러그인 아키텍처와 통합돼 GUI 기반 파라미터 설정, ROI 기반 자동 피팅, 배치 처리 파이프라인을 지원한다. 특히 DCE‑MRI 전용 플러그인은 Tofts, Extended Tofts, 2‑Compartment 모델 등을 미리 구현하고, AIF 추출·보정, 시간‑강도 곡선 정규화, 파라미터 매핑 시각화를 일괄 제공한다. 검증 단계에서는 기존 공개 디지털 팬텀(QIBA DCE‑MRI)과 자체 제작한 고해상도 시뮬레이션을 사용해 ground‑truth 파라미터와의 편차를 정량화했다. 결과는 평균 절대 오차가 5 % 이하이며, 기존 상용 소프트웨어와 비교해 유사하거나 더 낮은 편차를 보였다. 또한, 오픈소스 특성상 코드 리뷰와 CI 파이프라인을 통해 버그와 성능 회귀를 지속적으로 감시한다.
핵심 기여는 (1) 모델·피팅·결과를 완전 분리한 추상화 설계, (2) MITK와의 네이티브 통합을 통한 데이터 흐름 최적화, (3) 다양한 의료 영상 분야에 적용 가능한 플러그인 생태계 제공, (4) 오픈소스·플랫폼 독립성을 유지하면서도 고성능 연산을 지원하는 구현이다. 이러한 설계는 연구자들이 새로운 모델을 빠르게 프로토타이핑하고, 임상 현장에서 대규모 데이터에 자동화된 파라미터 추출을 적용하는 데 필요한 기술적 장벽을 크게 낮춘다.
댓글 및 학술 토론
Loading comments...
의견 남기기