노화·만성질환과 패혈증이 공유하는 혈관내피 기능장애의 핵심 메커니즘
초록
본 리뷰는 패혈증, 노화 및 주요 만성질환(고혈압, 당뇨, 심혈관·신장·폐·간 질환 등)에서 나타나는 혈관내피 기능장애(ED)의 공통된 특징을 정리한다. 저자들은 PubMed에 게재된 최근 10년 내 연구들을 중심으로 산화 스트레스·전신 염증, 글리코칼릭스 파괴, 세포간 접합소 해체·세포 사멸, 백혈구 부착·침윤 증가, 그리고 친응고·항섬유소용해 상태 유도라는 다섯 가지 핵심 메커니즘을 도출한다. 또한 만성질환이 내피 재생을 저해한다는 점을 강조하며, 기존 ED가 이미 존재하는 상태에서 급성 패혈증이 발생할 경우 손상이 증폭될 가능성을 제시한다.
상세 분석
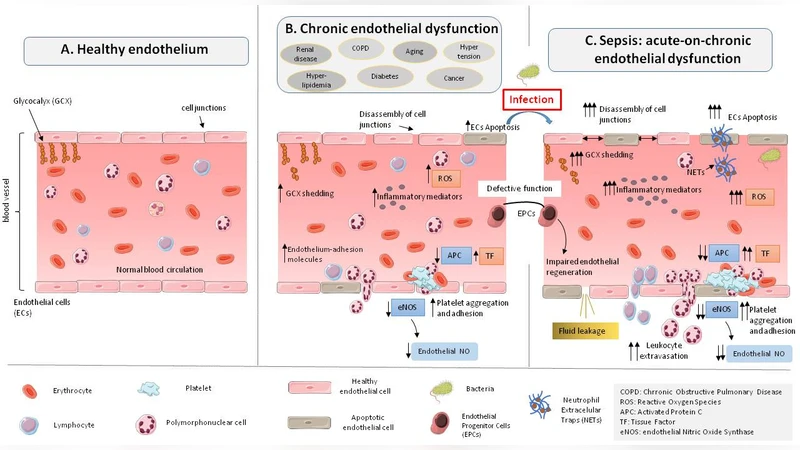
이 논문은 혈관내피가 정상 상태에서 수행하는 장벽·항응고·혈류조절 기능을 출발점으로 삼아, 패혈증, 노화, 그리고 다양한 만성질환이 어떻게 동일한 병리학적 경로를 통해 내피를 손상시키는지를 체계적으로 분석한다. 첫 번째로, 산화 스트레스와 전신 염증은 NADPH 산화효소, 미토콘드리아 ROS, 그리고 iNOS에 의한 과도한 NO 생산을 통해 내피세포의 기능을 억제한다. 특히, 노화와 당뇨, 고혈압 등에서 관찰되는 지속적인 ROS 증가는 eNOS 비활성화와 NO 생성을 감소시켜 혈관 확장을 방해하고, 혈소판·백혈구 부착을 촉진한다. 두 번째 메커니즘인 글리코칼릭스(GCX) 파괴는 혈관 내강을 보호하던 당단백질·당지질 복합체가 효소(헤파린분해효소, 히알루론산분해효소)와 염증 매개체에 의해 손실되는 과정이다. 임상적으로 혈중 syndecan‑1, heparan sulfate 등의 증가가 GCX 손상을 반영한다. 세 번째는 세포간 접합소(VE‑cadherin, claudin, occludin)의 해체와 내피세포 사멸이다. 패혈증에서는 PAMPs·DAMPs와 NETs가 직접적인 세포독성을 나타내며, 만성질환에서는 고지혈증·고당혈증이 접합소 단백질 발현을 억제한다. 네 번째는 백혈구 부착·침윤의 증가이다. 염증성 사이토카인(TNF‑α, IL‑1β)과 선택인자(P‑selectin, E‑selectin) 발현이 상승하면서, 혈관벽에 백혈구가 고정되고 조직으로 이동한다. 마지막으로, 친응고·항섬유소용해 상태는 조직인자(TF) 발현, thrombomodulin·protein C receptor 감소, 그리고 NETs가 제공하는 트롬빈·피브린 격자에 의해 강화된다. 이러한 다섯 축은 서로 상호보강적으로 작용해 혈관투과성 증가, 미세혈전 형성, 장기 저산소증을 초래한다. 논문은 또한 만성질환이 내피전구세포(Endothelial Progenitor Cells)의 수와 기능을 저하시켜 손상 회복을 방해한다는 점을 강조한다. 연구방법론 측면에서 저자들은 10년 이내 PubMed 논문을 중심으로 서술적 리뷰를 수행했으며, 표 1을 통해 대규모 코호트(>100,000명)에서의 연령·동반질환 비율을 제시한다. 그러나 메타분석이나 정량적 데이터 통합이 부족하고, 각 질환별 내피 손상의 정도를 비교하는 직접적인 임상시험 데이터가 제한적이다. 향후 연구는 기존 내피 기능지표(예: 혈중 syndecan‑1, angiopoietin‑2)와 패혈증 발생 위험을 연계한 전향적 코호트, 그리고 내피 재생을 촉진하는 치료제(예: EPC 강화제, GCX 보호제)의 임상시험이 필요하다.
댓글 및 학술 토론
Loading comments...
의견 남기기