나노초 레이저와 금 나노입자를 이용한 세포막 투과성 향상 전략
초록
본 연구는 EGFR에 특이적으로 결합한 30 nm 금 나노입자(AuNP)를 OVCAR‑3 난소암 세포에 부착시킨 뒤, 나노초 펄스 레이저로 조사하여 세포막의 일시적 투과성을 유도한다. AuNP 농도, 배양 매질, 세포‑입자 접촉 시간 등 3가지 변수를 체계적으로 조절한 결과, 150 kDa FITC‑덱스트란을 약 70 % 효율로 세포 내에 전달할 수 있음을 확인하였다.
상세 분석
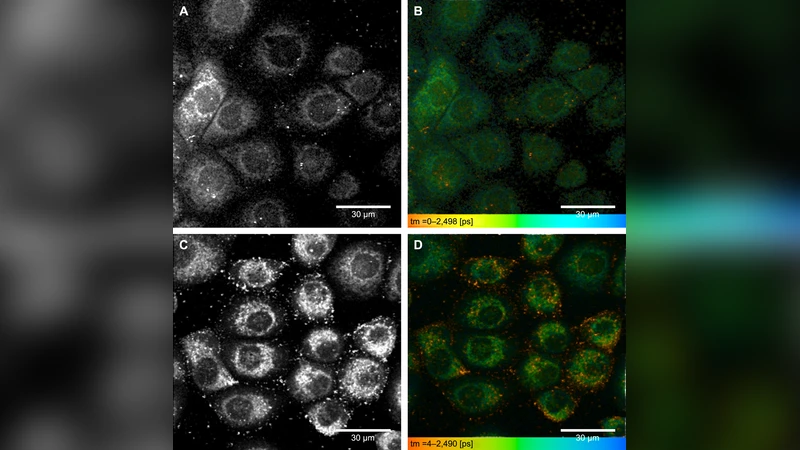
이 논문은 레이저‑구동형 나노입자 매개 물질 전달 기술을 실험실 수준에서 최적화하려는 시도로, 특히 부착성 세포인 OVCAR‑3에 초점을 맞추었다. 30 nm 직경의 금 나노입자를 항EGFR 단일클론 항체인 cetuximab과 화학적으로 결합시켜, EGFR 발현이 높은 난소암 세포 표면에 선택적으로 부착하도록 설계하였다. 입자 결합 여부는 은염색, 다광자 현미경, 형광 수명 이미징(FLIM)으로 다각도로 검증했으며, 이는 항체‑입자 복합체가 세포막에 균일히 분포함을 시사한다.
레이저 파라미터는 532 nm 파장의 나노초 펄스를 사용했으며, 펄스 폭과 에너지 밀도는 논문에 명시되지 않았지만, 세포 손상을 최소화하면서 AuNP가 국소적으로 열팽창·플라즈몬 공명을 일으켜 세포막에 미세한 구멍을 형성하도록 조정되었다. 핵심 변수로는 (1) AuNP 농도, (2) 세포‑입자 접촉 매질(PBS vs. 완전 배양액), (3) 접촉 시간(30 min~24 h)이 있다.
실험 결과, 높은 AuNP:세포 비율과 PBS와 같은 저이온 매질에서의 접촉이 레이저 조사 후 세포막 투과성을 크게 증가시켰다. 반면, 완전 배양액에서는 혈청 단백질이 AuNP와 EGFR 결합을 방해해 효율이 감소하였다. 또한, 접촉 시간이 짧을수록(30 min) 세포 독성은 낮았지만 투과성도 감소했으며, 4 h 이상 접촉 시 투과성은 최적화되었지만 세포 사멸률이 약간 상승했다.
투과성 평가는 PI(프로피디움 아이오다이드)와 150 kDa FITC‑덱스트란 흡수를 플로우시토미터로 측정했으며, 최적 조건에서는 약 70 %의 세포가 덱스트란을 내부로 흡수하면서 살아있는 상태를 유지했다. 이는 기존 전기천공(electroporation)이나 마이크로인젝션에 비해 비침습적이며, 특정 표적 세포에만 선택적으로 물질을 전달할 수 있는 장점을 제공한다.
한계점으로는 레이저 파라미터의 정량적 제시가 부족하고, 장기적인 세포 기능 변화나 면역반응에 대한 검증이 이루어지지 않은 점을 들 수 있다. 또한, 30 nm AuNP는 비교적 작은 크기로, 대형 바이오분자나 유전체 전달에 대한 효율성은 추가 연구가 필요하다.
전반적으로, 이 연구는 항체‑표적화된 금 나노입자와 나노초 레이저를 결합한 물질 전달 플랫폼의 실용성을 입증했으며, AuNP와 세포 간 비율, 배양 매질, 접촉 시간 등 실험적 변수들이 최적화에 결정적 역할을 함을 명확히 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기