혼합이론으로 보는 유방암 조직 내 용질 운반 메커니즘
초록
본 연구는 혼합이론을 이용해 유방암 조직 내 나노입자 및 용질의 운반을 모델링하고, 단일 모세관(SBC), 두 개의 평행 모세관(2 BC), 그리고 혈관과 림프관이 평행한 구조(BC_LC) 세 가지 혈관 구성을 비교하였다. 0.1 kDa부터 70 kDa까지 다섯 종류의 용질에 대해 시뮬레이션한 결과, 두 번째 모세관이 존재하면 조직 내 농도가 감소하고, 림프관이 추가되면 감소폭이 더욱 커졌다. 흐름 방향에 따라 큰 입자는 비균일하게 분포하고, 작은 입자는 역류 흐름에서 국소적으로 포획되는 현상이 관찰되었다. 또한, 비차원 시간 척도 T*ₚₑₐₖ≈0.027±0.018이 모든 조건에서 동일하게 나타나, 치료 시점 예측에 활용될 수 있음을 제시한다.
상세 분석
본 논문은 종양 미세환경에서 용질(특히 나노입자)의 전달을 정량적으로 이해하기 위해 혼합이론(mixture theory)을 기반으로 한 연속체 모델을 구축하였다. 혼합이론은 혈관 내 혈액, 조직 간질, 그리고 용질(또는 입자) 각각을 별개의 상(phase)으로 간주하고, 각 상의 질량·운동량 보존 방정식을 상호 결합시켜 전체 시스템을 기술한다. 이를 통해 혈관 내 대류·확산, 혈관벽을 통한 투과, 조직 내 확산·흡착, 그리고 림프관 배출이라는 복합적인 메커니즘을 하나의 수학적 틀 안에 포함시킬 수 있다.
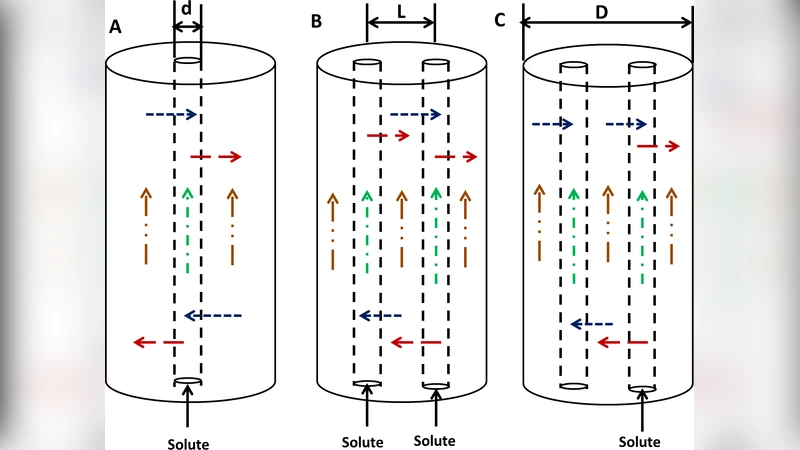
모델링에서는 원통형 조직 블록을 가정하고, 중심축에 단일 모세관(SBC)을 배치한 경우와, 동일한 반경을 갖는 두 개의 평행 모세관(2 BC), 그리고 혈관과 동일한 직경의 림프관이 병렬로 존재하는 경우(BC_LC)를 비교하였다. 각 혈관은 일정한 평균 유속을 갖는 전형적인 Poiseuille 흐름을 가정했으며, 혈관 내 용질 농도는 입구에서 일정 농도 C₀로 설정하고, 출구에서는 완전 혼합(Neumann 경계)으로 처리하였다. 혈관벽 투과는 Starling 법칙을 변형한 형태로 모델링했으며, 투과계수는 용질 분자량에 따라 실험적으로 추정된 스케일링 법칙을 적용하였다. 조직 내에서는 용질이 확산계수 D와 조직 간질의 체적비 φ에 의해 지배되며, 큰 입자(≥30 kDa)의 경우 조직 매트릭스와의 물리적 포획(adsorption) 효과를 추가적인 소실항으로 구현하였다.
시뮬레이션 결과는 다음과 같은 핵심 인사이트를 제공한다. 첫째, 두 번째 모세관이 존재하면 조직 내 평균 농도가 약 10–30 % 감소한다(2 BC). 이는 인접 혈관 간의 용질 경쟁 효과와 혈관벽을 통한 투과 면적 증가가 복합적으로 작용한 결과로 해석된다. 둘째, 림프관이 추가된 BC_LC 구성에서는 농도 감소폭이 45–60 %에 달한다. 림프관은 조직 내 용질을 빠르게 제거하는 배출 경로를 제공함으로써, 특히 고분자 용질에서 그 효과가 두드러진다. 셋째, 혈류 방향에 따른 비대칭 현상이 관찰되었다. 두 모세관이 동류(co‑current) 흐름일 경우, 큰 입자(≥30 kDa)는 혈관 사이의 간격 부근에 고농도 영역을 형성해 비균일한 분포를 만든다. 반대로 역류(counter‑current) 흐름에서는 작은 입자(0.1 kDa, 3 kDa)가 혈관 간격 중앙에 국소적으로 포획되는 현상이 나타나, 혈류 패턴이 입자 크기에 따라 조직 내 체류 시간을 크게 조절함을 시사한다.
또한 저자들은 여러 기하학적·물리적 파라미터(혈관 직경, 간격, 용질 확산계수, 투과계수 등)를 비차원화하여 통합 시간 척도 T* = t·(k·A)/(V·C₀) 형태의 식을 도출하였다. 흥미롭게도 모든 시뮬레이션 케이스에서 최고 농도 피크가 T*ₚₑₐₖ≈0.027±0.018에서 발생했으며, 이는 용질 크기, 혈관 배열, 흐름 방향에 무관한 보편적 현상으로 해석된다. 이 비차원 피크 시간은 실제 치료 시점—예를 들어 약물 방출 트리거나 광열 치료용 레이저 조사—을 최적화하는 데 직접 활용될 수 있다.
마지막으로 논문은 모델의 한계도 언급한다. 조직을 균질한 원통형으로 가정했으며, 혈관벽의 복합적인 구조(내피세포, 기저막, 주변 근육층)와 동적 혈류 변동성(펄스 흐름, 혈관 수축)을 고려하지 않았다. 또한 용질-조직 상호작용을 단순화한 점(흡착을 1차 소실항으로만 모델링)도 실제 종양 미세환경에서의 복잡한 결합/해리 반응을 충분히 반영하지 못한다. 그럼에도 불구하고, 혼합이론 기반 모델이 다양한 혈관 구성을 정량적으로 비교하고, 비차원 피크 시간을 도출함으로써 종양 내 약물 전달 설계에 실용적인 가이드를 제공한다는 점에서 큰 의미가 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기