선형 회귀와 피어슨 상관계수를 활용한 암 특이 유전자 조절망 예측
초록
본 연구는 암 조직의 마이크로어레이 데이터를 이용해 두 단계의 간단한 머신러닝 파이프라인을 구축한다. 첫 단계에서는 선형 회귀 분석으로 발현 변동이 큰 유의미한 유전자를 선별하고, 두 번째 단계에서는 피어슨 상관계수를 계산해 이들 유전자 간의 조절 관계를 추정한다. 얻어진 네트워크는 기존 데이터베이스와 문헌을 통해 검증했으며, 허브 유전자를 식별해 암 진단 및 치료 표적으로 활용 가능성을 제시한다.
상세 분석
이 논문은 유전자 발현 프로파일을 기반으로 암 특이적인 유전자 조절망(GRN)을 구축하기 위해 ‘선형 회귀 → 피어슨 상관’이라는 두 단계의 순차적 접근법을 제안한다. 첫 단계에서 선형 회귀 모델을 적용해 각 유전자의 발현값을 종속 변수로 두고, 다른 모든 유전자를 독립 변수로 사용함으로써 회귀계수의 절대값이나 p‑값을 기준으로 ‘특이하게 변동하는’ 유전자를 추출한다. 이 과정은 변수 선택(feature selection) 차원에서 LASSO나 Elastic Net과 같은 정규화 기법을 도입하지 않아 과적합 위험이 존재한다는 점이 아쉽다. 또한, 선형 회귀는 변수 간의 선형 관계만을 모델링하므로 비선형 상호작용이나 복합적인 조절 메커니즘을 포착하지 못한다.
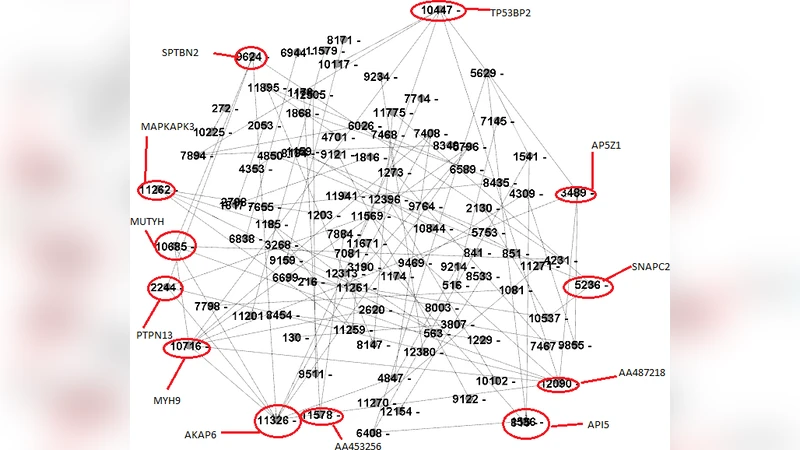
두 번째 단계에서는 선택된 유전자 쌍 간의 피어슨 상관계수를 계산해 상관값이 사전 정의된 임계값(예: |r| > 0.8)을 초과하는 경우에만 엣지를 부여한다. 피어슨 상관은 순수히 선형 상관성을 측정하므로, 실제 생물학적 조절 관계가 비선형이거나 시간 지연을 포함하는 경우에는 놓치게 된다. 더구나 상관계수는 인과성을 제공하지 않으며, 공통 조절인자에 의해 발생하는 ‘공통 원인 효과’를 구분하지 못한다. 따라서 이 방법으로 구축된 네트워크는 ‘공동 발현’ 네트워크에 가깝고, 전통적인 GRN이 요구하는 방향성(directed)과 조절 유형(activation/inhibition)을 반영하지 못한다.
검증 단계에서는 기존의 공공 데이터베이스(예: STRING, BioGRID)와 문헌에 보고된 암 관련 유전자 리스트와 비교했지만, 정량적 성능 지표(예: 정밀도, 재현율, AUC)가 제시되지 않아 실제 예측 정확도를 평가하기 어렵다. 또한, 교차 검증이나 독립 테스트 세트를 이용한 일반화 검증이 누락돼 모델의 재현 가능성을 의심하게 만든다.
이러한 한계에도 불구하고, 논문은 매우 간단한 파이프라인으로도 암 관련 허브 유전자를 식별할 수 있음을 시연한다는 점에서 실용적 가치를 제공한다. 특히, 대규모 컴퓨팅 자원이 제한된 연구 환경에서 빠른 초기 탐색 단계로 활용될 수 있다. 향후 연구에서는 (1) LASSO/Elastic Net 등 정규화 회귀를 통한 변수 선택, (2) 부분 상관(partial correlation)이나 그래프 라쏘(Graphical Lasso)와 같은 고차원 상관 추정 기법, (3) 베이지안 네트워크, 동적 베이즈 네트워크, 혹은 딥러닝 기반 인과 추론 모델을 도입해 방향성과 비선형성을 포착하고, (4) 독립적인 검증 코호트와 ROC‑AUC 등 정량적 지표를 제시함으로써 결과의 신뢰성을 강화할 필요가 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기