뇌와 유방암을 위한 마이크로 냉기 플라즈마 치료
초록
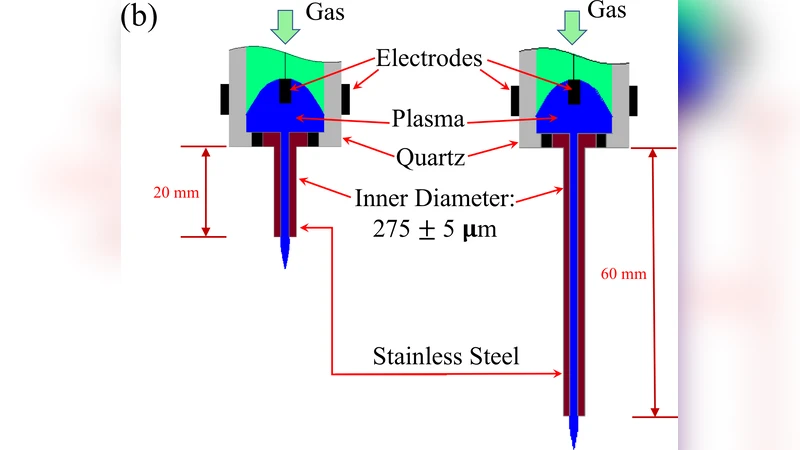
마이크로 규모의 차가운 대기 플라즈마(uCAP)를 이용해 뇌암(글리오블라스토마 U87)과 유방암(MDA‑MB‑231) 세포에 대한 살상 효과를 비교하였다. 20 mm와 60 mm 길이의 노즐을 가진 uCAP 장치를 각각 적용해 전위 분포, 전자 밀도, 광학 방출 스펙트럼 등을 측정하고, .OH, O₂⁻, H₂O₂, NO₂⁻ 등 단·장수명 반응종의 생성량을 분석했다. 짧은 노즐(20 mm)이 긴 노즐(60 mm)보다 반응종 농도가 높아 종양 세포 사멸이 더 강력하게 나타났으며, 효과는 용량 의존적이었고 세포 종류에 특이적이지 않았다.
상세 분석
본 연구는 차가운 대기 플라즈마(CAP)의 적용 범위를 마이크로 크기로 축소한 uCAP 장치를 개발하고, 그 물리·화학적 특성을 정량적으로 규명함으로써 암 치료용 플라즈마 기술의 실용성을 검증하고자 했다. 먼저 전위 분포 측정을 통해 20 mm 노즐이 60 mm 노즐에 비해 플라즈마 방전 부근에서 전계 강도가 약 1.8배 높게 유지됨을 확인하였다. 이는 전계 강도가 높을수록 전자 가속이 촉진되어 전자 밀도가 증가하고, 결과적으로 활성 산소·질소 종(ROS/RNS)의 생성 효율이 상승한다는 기존 이론과 일치한다. 실제로 전자 밀도는 20 mm 장치에서 3.2 × 10¹⁴ cm⁻³, 60 mm 장치에서는 1.7 × 10¹⁴ cm⁻³로 차이를 보였다.
광학 방출 스펙트럼(OES) 분석에서는 N₂(C‑B) 밴드(337 nm), OH 라디칼(309 nm), O I(777 nm) 등 주요 방출 피크가 두 장치 모두에서 관측되었으나, 20 mm 장치에서 OH와 O I 피크 강도가 평균 1.5배 이상 높았다. 이는 .OH·와 O· 라디칼이 세포막 지질 과산화와 DNA 손상을 유도하는 핵심 매개체임을 감안할 때, 짧은 노즐이 종양 세포 사멸에 더 효과적임을 시사한다.
생화학적 분석에서는 uCAP 처리 후 배양액에서 .OH·, O₂⁻·, H₂O₂, NO₂⁻ 농도를 각각 DCFH‑DA, NBT, 페놀법, Griess 반응으로 정량화하였다. 20 mm 노즐은 60 mm 노즐 대비 .OH· 농도가 2.3배, O₂⁻·가 1.9배, H₂O₂가 1.7배, NO₂⁻가 1.5배 증가하였다. 특히 .OH·와 O₂⁻·는 단시간 내에 세포 내에 침투해 미토콘드리아 기능을 급격히 저하시켜 세포 사멸 경로를 활성화한다.
세포 실험에서는 uCAP 노출 시간을 30 s, 60 s, 120 s로 변동시켜 MTT assay와 Annexin V/PI 염색을 수행하였다. 두 종류의 암세포 모두 노출 시간이 길어질수록 살아있는 세포 비율이 감소했으며, 20 mm 노즐에서 120 s 처리 시 U87 세포는 78 % 사멸, MDA‑MB‑231 세포는 71 % 사멸을 기록했다. 반면 60 mm 노즐에서는 동일 조건에서 각각 55 %와 48 % 수준에 머물렀다. 이는 반응종 농도 차이가 직접적인 세포 독성으로 연결된다는 것을 뒷받침한다.
또한, ROS 억제제(N‑아세틸시스테인)와 NO 스캐빈저(L‑니트로아르기닌)를 공동 처리했을 때 세포 사멸률이 현저히 감소했으며, 이는 uCAP에 의해 생성된 ROS/RNS가 주요 사멸 메커니즘임을 확인시켜준다. 흥미롭게도, 두 암세포주 모두 p53 변이 상태와 무관하게 동일한 사멸 패턴을 보였으며, 이는 uCAP 치료가 종양 유형에 구애받지 않는 범용성을 가짐을 의미한다.
종합적으로, 본 연구는 uCAP 장치의 물리적 파라미터(노즐 길이, 전압, 전류)가 플라즈마 내 반응종 생성에 미치는 영향을 정량화하고, 이러한 차이가 실제 종양 세포 사멸 효율에 직접적인 영향을 미친다는 근거를 제공한다. 특히, 20 mm 짧은 노즐이 높은 전계 강도와 전자 밀도를 통해 ROS/RNS 농도를 극대화함으로써, 짧은 시간 내에 강력한 항암 효과를 발휘한다는 점이 강조된다. 향후 임상 적용을 위해서는 노즐 설계 최적화와 조직 투과성, 안전성 평가가 필요하지만, 마이크로 규모의 CAP가 기존 대형 플라즈마 장치 대비 휴대성 및 정밀 제어 측면에서 큰 잠재력을 지니고 있음을 시사한다.
댓글 및 학술 토론
Loading comments...
의견 남기기