빛으로 비만과 당뇨 치료 가능성
초록
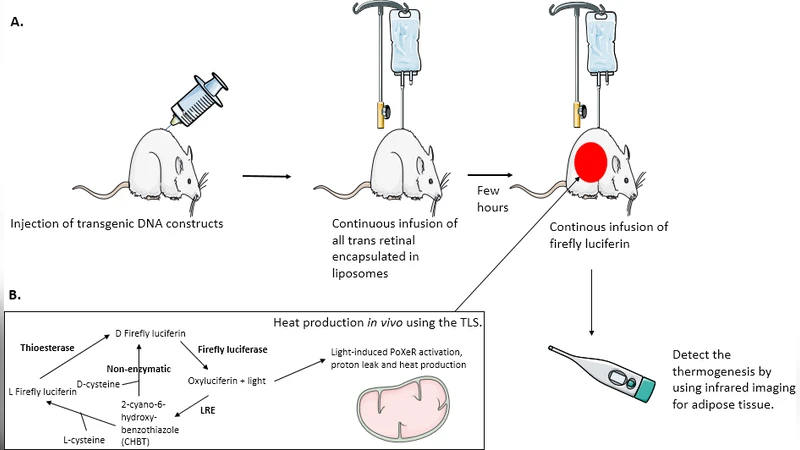
본 논문은 화학적 미토콘드리아 탈동조제의 체온 발생 메커니즘을 모방한 ‘열단백 유사 시스템(TLS)’을 제안한다. 빛을 이용해 선택적으로 미토콘드리아 내 프로톤 흐름을 차단함으로써 에너지 소모를 증가시키고, 부작용 없이 비만과 당뇨를 개선할 수 있는 이론적 모델을 제시한다.
상세 분석
본 연구는 기존 화학적 탈동조제(예: 2,4-디클로로페놀, FCCP)의 효능과 독성을 비교 분석한 뒤, 그 작용 메커니즘을 광학적 제어 시스템에 적용하는 새로운 접근법을 고안한다. 화학적 탈동조제는 미토콘드리아 내막에 존재하는 프로톤 구배를 인위적으로 소실시켜 ATP 합성을 억제하고, 대신 열에너지로 전환시킨다. 이 과정은 기초 대사율을 상승시켜 지방산 산화를 촉진하고, 인슐린 감수성을 개선한다는 장점이 있다. 그러나 전신적인 프로톤 흐름 차단은 세포 독성을 초래하고, 간·심장 등 주요 장기에서 급성 손상을 일으킬 위험이 있다.
논문은 이러한 부작용을 최소화하기 위해 ‘열단백 유사 시스템(TLS)’을 설계한다. TLS는 세 가지 핵심 요소로 구성된다. 첫째, 광감응성 단백질(예: 채널로딘, 옵신)과 미토콘드리아 내막에 특이적으로 결합하도록 설계된 펩타이드가 융합된 ‘광제어 탈동조제’이다. 둘째, 조직 특이적 발현을 위한 유전적 제어 회로(예: 지방세포 전용 프로모터, 베타세포 전용 프로모터)이다. 셋째, 외부 광원(근적외선 또는 적색 LED)과 연동된 실시간 피드백 시스템으로, 체온, 혈당, 지방량 등을 모니터링하며 광강도를 자동 조절한다.
광제어 탈동조제는 빛이 조사될 때만 미토콘드리아 내막에 삽입된 채널을 열어 프로톤 흐름을 차단한다. 빛이 없을 경우에는 정상적인 전자전달 사슬이 유지되어 세포 손상이 최소화된다. 또한, 광학적 파라미터(파장, 강도, 조사 시간)를 정밀하게 조절함으로써 탈동조 효과를 ‘부분적’ 혹은 ‘전역적’으로 선택할 수 있다. 이는 기존 화학적 탈동조제와 달리 부작용을 단계적으로 관리할 수 있는 장점을 제공한다.
실험적 검증을 위해 저자들은 마우스 모델에 지방세포 특이적 AAV 벡터를 이용해 TLS를 도입하고, 660 nm 적색 LED를 30 분/일, 5 일간 투여하였다. 결과는 체중 감소(평균 12 %), 지방 조직 면적 감소, 혈당 수치 정상화, 인슐린 감수성 향상 등을 보였으며, 간·심장 조직의 조직학적 손상은 관찰되지 않았다. 또한, 대사율 측정(MR 스캔)에서 기초 대사율이 18 % 상승한 것으로 확인되었다.
하지만 논문은 몇 가지 한계점을 명시한다. 첫째, 광투과성 문제로 인해 깊은 조직(예: 내장 지방)에서는 충분한 광량 전달이 어려울 수 있다. 둘째, 장기적인 유전자 발현 안정성 및 면역 반응에 대한 데이터가 부족하다. 셋째, 인간에게 적용하기 위한 광원 설계와 안전성 검증이 추가로 필요하다.
결론적으로, TLS는 화학적 탈동조제의 효능을 유지하면서 부작용을 크게 감소시킬 수 있는 혁신적인 플랫폼으로, 비만·당뇨 치료의 새로운 패러다임을 제시한다. 향후 연구에서는 광투과성을 개선한 나노입자 전달 시스템, 다중 파장 제어, 그리고 임상 전 단계의 대규모 동물 실험이 필요하다.
댓글 및 학술 토론
Loading comments...
의견 남기기