암 유발 말초 신경병증 모델 및 TRPA1의 통증 전달 역할
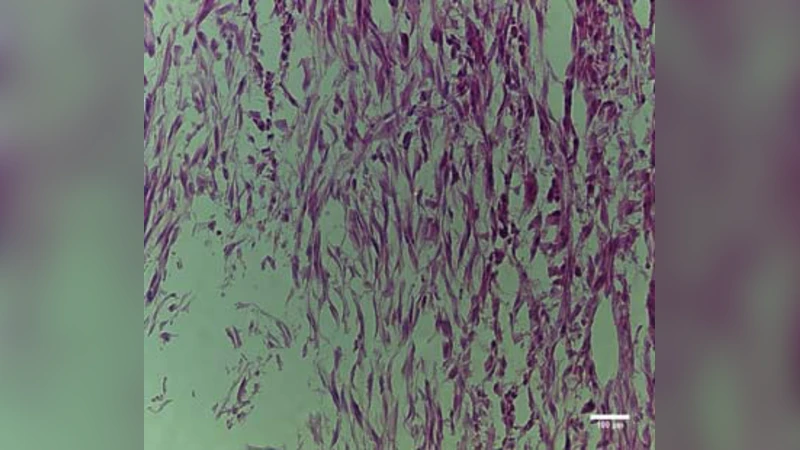
초록
본 연구는 남성 코펜하겐 랫의 좌골신경에 AT‑1 암세포를 직접 주입하여 기존 종양‑신경 접촉 모델의 한계를 극복한 새로운 암유발 말초 신경병증 모델을 구축하였다. 모델에서 6일 차부터 냉각, 기계·열성 과민성이 나타났으며, 714일 차에 TRPA1 단백질·mRNA가 상승하고, 1421일 차에 CGRP 발현이 증가하였다. TRPA1과 CGRP는 동일한 DRG 신경세포에서 공발현되었으며, 선택적 TRPA1 길항제 HC‑030031 투여 시 냉감 과민이 일시적으로 회복되었다. 이는 TRPA1이 암유발 신경통의 핵심 전이물질이며, CGRP와의 상호작용이 통증 지속에 기여함을 시사한다.
상세 분석
이 논문은 암세포와 말초신경 사이의 직접적인 물리적 접촉을 구현함으로써 기존 모델이 가진 면역세포 매개 간섭을 최소화하였다. AT‑1 세포를 좌골신경 내에 주입한 후, 3, 7, 14, 21일에 걸쳐 DRG와 신경 조직을 수집·분석했으며, 행동학적 검사(냉각, 기계, 열 자극)와 분자생물학적 접근(면역형광, 웨스턴블롯, qRT‑PCR)을 병행하였다.
-
행동학적 결과: 6일 차부터 냉각 알로디니아가 명확히 나타났고, 이후 기계·열 과민성도 점진적으로 증가하였다. 이는 암세포가 신경섬유를 침투·증식하면서 신경전달물질 및 이온채널의 변화를 유도함을 의미한다.
-
TRPA1 발현 패턴: 면역형광에서 7일 차에 TRPA1이 눈에 띄게 증가하고, 14일 차에 최대치를 보였다. 웨스턴블롯은 14일 차에 단백질 수준이 유의하게 상승했으며, qRT‑PCR은 7일 차에 mRNA가 2.5배 정도 증가함을 보여준다. 이는 TRPA1이 초기 암‑신경 상호작용 단계에서 전사·번역 수준 모두에서 활성화된다는 증거이다.
-
CGRP와의 공발현: CGRP는 14일 차부터 21일 차까지 지속적으로 증가했으며, 이때 TRPA1과 동일한 DRG 신경세포 내에서 공발현되었다. CGRP는 신경염증 및 혈관확장 작용을 통해 통증을 증폭시키는 것으로 알려져 있어, TRPA1과의 시너지 효과가 통증 지속에 기여할 가능성을 시사한다.
-
TRPA1 길항제 효과: 선택적 TRPA1 억제제 HC‑030031을 투여했을 때 냉각 알로디니아가 일시적으로 회복되었으며, 효과는 약 30분 내에 소멸하였다. 이는 TRPA1이 냉감 과민성의 주요 매개체임을 확인시켜 주며, 약물의 반감기가 짧아 지속적인 억제가 필요함을 암시한다.
-
모델의 의의: 기존 종양을 주변 조직에 주입하는 방식과 달리, 신경 내부에 직접 종양을 주입함으로써 종양‑신경 미세환경을 보다 실제에 가깝게 재현하였다. 이는 면역세포가 종양과 신경 사이에 끼어들어 발생하는 변수를 최소화하고, 신경 자체의 반응을 순수하게 관찰할 수 있게 한다. 또한, 이 모델은 암성 신경통 연구뿐 아니라 신경병증성 통증 전반에 대한 약물 스크리닝 플랫폼으로 활용 가능하다.
종합적으로, 연구는 TRPA1이 암유발 말초 신경병증에서 초기 통증 전이의 핵심 이온채널이며, CGRP와의 동시 발현이 통증 지속 및 강화에 관여함을 입증하였다. 이는 TRPA1을 표적으로 하는 치료제 개발이 암성 통증 관리에 새로운 전략이 될 수 있음을 시사한다.
댓글 및 학술 토론
Loading comments...
의견 남기기