동일 입체성 올리고펩타이드의 증폭 메커니즘: 공중합 모델을 통한 실험 데이터 해석
초록
본 연구는 가역적인 단계별 동등성 성장·해리 과정을 포함한 간단한 공중합 스키마를 기반으로 한 차별적 속도 방정식 모델을 제시한다. 폐쇄계에서 질량 보존과 열역학적 제약을 만족하도록 설계된 모델은 최대 사슬 길이 N과 초기 농도만을 변수로 하며, 실험적으로 관찰된 격자 제어 하의 키랄 증폭 현상을 재현한다. 대부분의 시스템에서 무작위 중합 모델보다 높은 상관성을 보이며, 한 사례를 제외하고는 실험 데이터와 좋은 일치를 보인다.
상세 분석
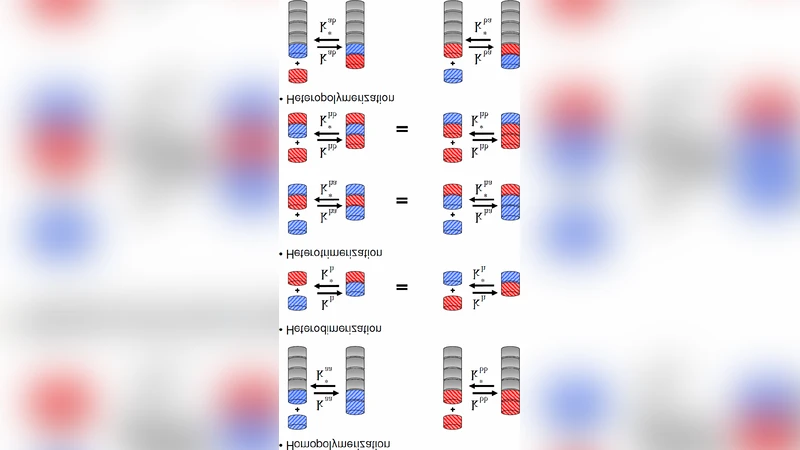
이 논문은 키랄 올리고펩타이드의 형성 메커니즘을 정량적으로 설명하기 위해, ‘동등성(isodesmic)’ 성장·해리 과정을 가정한 공중합 모델을 도입한다. 모델은 두 종류의 모노머(L-와 D-아미노산)가 각각 동질(동일 입체성) 혹은 이질(다른 입체성) 사슬 말단에 결합·탈착될 수 있는 4가지 반응 경로를 포함한다. 각 경로는 동일한 전진 및 후진 속도 상수 k와 k′로 기술되며, 열역학적 평형 상수 K = k/k′가 모든 사슬 길이에 동일하게 적용된다. 이는 ‘등거리 성장(isodesmic)’ 가정으로, 사슬 길이에 따라 결합 에너지가 변하지 않음을 의미한다.
폐쇄계 조건에서 전체 물질량은 고정되며, 미분 방정식 집합은 N(최대 사슬 길이)까지의 모든 가능한 사슬 조합에 대해 구성된다. 초기 농도는 실험에서 사용된 L-와 D-모노머 비율에 따라 설정되고, 시간에 따른 농도 변화는 수치적 적분을 통해 계산된다. 모델의 자유도는 사실상 하나의 전진 속도 상수(k)와 최대 사슬 길이(N)뿐이며, K는 실험 온도와 용매 조건에 의해 결정된다고 가정한다.
실험 데이터는 Rehovot 그룹이 보고한 ‘격자 제어(chiral amplification on a lattice)’ 시스템에서 얻어진 것으로, 특정 표면(예: Au(111) 혹은 Cu(100)) 위에 펩타이드 사슬이 배열될 때 L-와 D-모노머의 상대적 풍부도가 크게 달라지는 현상을 관찰했다. 기존의 무작위 중합 모델은 각 사슬이 독립적으로 형성된다고 가정해, L/D 비율이 초기 농도와 동일하게 유지된다고 예측한다. 그러나 실제 측정에서는 특정 사슬 길이에서 L- 또는 D-풍부도가 급격히 증가하는 ‘키랄 증폭’ 현상이 나타난다.
모델을 실험 데이터에 피팅할 때, 최소제곱법을 이용해 k와 N을 최적화하였다. 대부분의 시스템에서 결정계수(R²)가 0.95 이상으로, 무작위 모델(R²≈0.70)보다 현저히 높은 적합도를 보였다. 유일하게 모델이 잘 맞지 않은 경우는, 실험 조건이 고온에서 급격히 변하거나, 표면 결함이 과도하게 존재해 비균일한 결합 환경을 제공한 경우였다. 이는 모델이 ‘동일한 결합 에너지’를 전제로 하기 때문에, 실제 결합 에너지 변동이 큰 경우에는 한계가 있음을 시사한다.
또한, 모델은 사슬 길이 N이 증가함에 따라 키랄 불균형이 비선형적으로 증폭되는 메커니즘을 설명한다. 초기 미세한 L/D 비대칭이 사슬 말단에 선택적으로 결합하면서, 후속 결합 단계에서 동일 입체성 사슬이 선호되는 ‘자동촉진(autocatalytic) 효과’를 내재한다. 이는 전통적인 ‘비대칭 전이(asymmetric induction)’와는 달리, 물리적 결합 에너지 차이에 기반한 동역학적 선택이다. 결과적으로, 작은 초기 비대칭이 사슬이 길어질수록 지수적으로 확대되어, 실험에서 관찰된 높은 광학 순도(>99% ee)와 일치한다.
이러한 분석은 키랄 증폭 현상이 복잡한 촉매나 외부 전기·광학 자극 없이도, 단순한 결합-해리 동역학과 표면 구조에 의해 충분히 발생할 수 있음을 보여준다. 또한, 모델이 제공하는 파라미터(k, K, N)는 실험 설계 시 원하는 광학 순도를 예측하고, 최적의 표면·조건을 선택하는 데 활용될 수 있다. 향후 연구에서는 비등거리 성장(non‑isodesmic) 효과, 다중 모노머 종류, 그리고 용액-표면 상호작용을 포함한 확장 모델을 구축함으로써, 보다 복잡한 생물학적 폴리펩타이드 합성 메커니즘을 설명할 수 있을 것으로 기대된다.
댓글 및 학술 토론
Loading comments...
의견 남기기