ATP 의존성 크로마틴 리모델링이 비접촉 전사인자 협동에 미치는 새로운 메커니즘
초록
이 논문은 마우스 유방암 바이러스(MMTV) 프로모터에서 글루코코르티코이드 수용체(GR)와 NF1/Oct‑1이 순차적으로 결합하는 과정을 재해석한다. 저자는 ATP‑의존성 SWI/SNF 리모델링 효소가 비가역적인 크로마틴 전환을 도입함으로써, 전통적인 평형 모델에서 발생하는 ‘트래핑’ 문제를 회피하고, 비접촉 전사인자 간의 협동성을 비평형적으로 설명할 수 있음을 보인다. 모델링 결과는 크로마틴 개방·폐쇄 속도비(β)와 결합 상수 비(α)가 프로모터의 시그모이드 반응과 감수성을 조절한다는 점을 강조한다.
상세 분석
본 연구는 전사인자 협동성을 설명하기 위해 두 가지 이론적 프레임워크를 비교한다. 첫 번째는 전통적인 미시적 가역성(미세평형) 가정에 기반한 모델로, GR(A)과 NF1/Oct‑1(B)이 순차적으로 결합하지만, 한 번 결합된 전사인자는 다른 전사인자가 탈착될 때까지 ‘트래핑’되는 현상을 보인다. 실험적으로는 GR이 언제든지 DNA에서 해리될 수 있음에도 불구하고, 이 모델은 GR이 포화된 상태에서 탈락이 불가능하다는 모순을 낳는다.
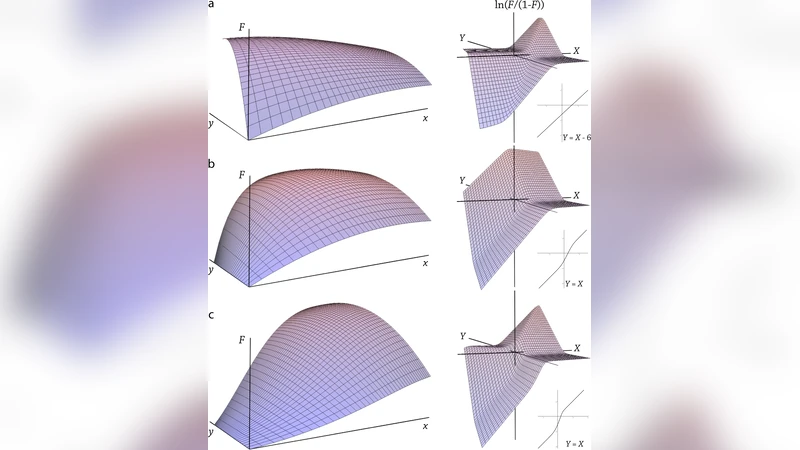
두 번째는 ATP‑의존성 크로마틴 리모델링 효소(SWI/SNF)를 도입한 비평형 모델이다. 여기서는 두 가지 크로마틴 상태 P(열린)와 P₀(닫힌)를 정의하고, GR이 두 상태에 각각 다른 결합 상수(K_A, K₀_A)를 가진다고 가정한다. 핵심은 ‘크로마틴 개방(k_o)’과 ‘크로마틴 폐쇄(k_c)’ 전이가 에너지 소모를 동반하는 비가역적 과정이며, 이 전이 속도비 β = k_o/k_c가 전사인자 결합 확률에 비선형적인 영향을 미친다.
수식 전개에 따르면, P 상태에서의 GR 결합 확률 p(A|P)와 P₀ 상태에서의 결합 확률 p(A|P₀)는 각각 K_A
댓글 및 학술 토론
Loading comments...
의견 남기기