RNA와 DNA 통합 분석을 통한 체세포 변이 탐지
초록
RADIA는 환자별 정상·종양 DNA와 종양 RNA를 동시에 활용해 체세포 단일염기 변이를 탐지하는 파이프라인이다. RNA 정보를 결합함으로써 낮은 DNA 대립유전자 비율에서도 변이를 회복(rescue)할 수 있어 민감도가 84%, 특이도가 98~99%에 달한다. TCGA 자궁내막암·폐선암 데이터와 인공 변이 시뮬레이션을 통해 성능을 검증했으며, 주요 암 유전자 변이도 추가로 발견했다.
상세 분석
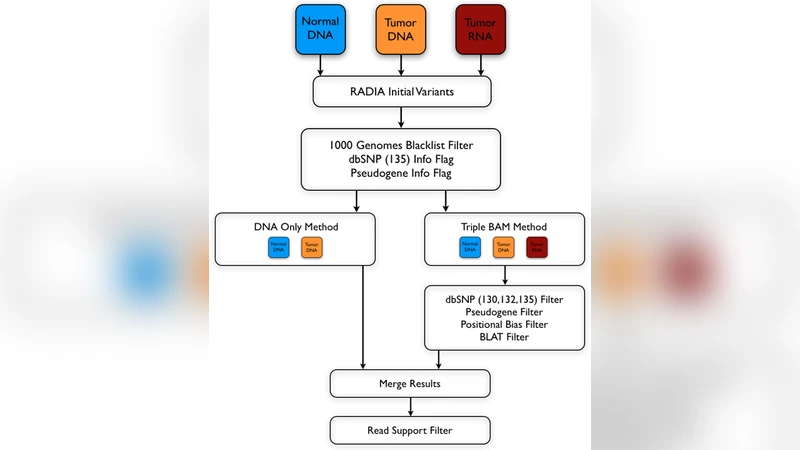
RADIA는 기존 DNA‑only 변이 검출기와 달리, 동일 환자에서 추출한 정상 DNA, 종양 DNA, 그리고 종양 전사체(RNA) 데이터를 통합 분석한다. 핵심 아이디어는 RNA에서 확인되는 변이가 DNA에서 낮은 알레일 빈도(예: 5% 이하)로 인해 DNA‑only 파이프라인에서 누락될 가능성을 보완한다는 점이다. 이를 위해 먼저 각각의 샘플에 대해 GATK와 MuTect 같은 표준 변이 호출기를 적용해 후보 변이 리스트를 만든다. 이후 RNA‑seq 데이터에서 동일 위치의 리드가 존재하는지 확인하고, RNA에서 최소 3개의 변이 리드와 최소 10% 변이 비율을 만족하는 경우를 ‘RNA‑supported’ 변이로 분류한다. 변이의 신뢰성을 높이기 위해 변이 주변의 매핑 품질, 베이스 품질, 스트랜드 편향 등을 추가 필터링한다.
특히 RADIA는 시뮬레이션 패키지를 제공한다. 이 패키지는 실제 TCGA 샘플에 인공 변이를 삽입해 ‘스파이크‑인’ 방식으로 민감도를 평가한다. DNA 알레일 빈도가 5% 이하인 상황에서도 RNA 지원을 통해 30% 이상 변이를 회복할 수 있음을 보여준다. 실제 TCGA 데이터에서는 자궁내막암(EC)와 폐선암(LUAD)에서 각각 84%와 86%의 민감도, 98%와 99%의 특이도를 기록했다. 특히 DNA와 RNA 모두에서 높은 리드 수와 변이 비율을 보인 변이는 검증율이 99%에 달했다.
임상적 의미 측면에서, RADIA는 TP53, KRAS, PIK3CA 등 주요 암 유전자에서 DNA‑only 분석에 비해 추가 변이를 발견했다. 이는 치료 표적 선정이나 예후 예측에 직접적인 영향을 미칠 수 있다. 또한, RNA‑level 변이 표현을 확인함으로써 변이가 실제 전사체에 반영되는지를 검증할 수 있어, 기능적 해석에 유리하다.
한계점으로는 RNA‑seq 데이터의 품질에 크게 의존한다는 점이다. 낮은 표현량 유전자나 RNA 편집 현상이 있는 경우 거짓 양성 또는 거짓 음성이 발생할 수 있다. 또한, DNA와 RNA 샘플 간의 시간적 차이(예: 조직 채취 시점 차이)로 인해 클론 확장 정도가 달라질 가능성도 존재한다. 향후에는 DNA‑RNA 정량적 통합 모델을 도입해 변이의 클론성 추정과 기능적 영향을 동시에 평가하는 방향이 제시된다.
댓글 및 학술 토론
Loading comments...
의견 남기기