세균 열충격 반응 회로가 기능적 유사성을 설명한다
초록
본 연구는 그람음성 대장균(E. coli)의 σ32 기반 열충격 체계와 그람양성 유산균(L. lactis)의 HrcA 기반 체계를 수학적으로 모델링한다. 두 시스템은 서로 다른 전사인자 조절 메커니즘을 갖지만, 부정적 피드백을 통해 유사한 동적 특성을 보인다. 모델 분석을 통해 σ32‑DnaK 결합 친화도는 100 nM 수준으로 제한을 두고, HrcA‑GroE 결합은 마이크로몰 농도까지 확장돼야 함을 밝혀냈다.
상세 분석
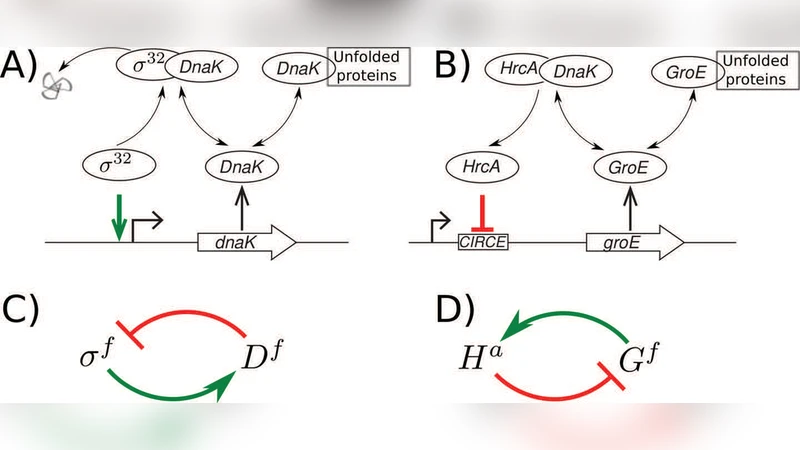
이 논문은 세균의 열충격 반응을 두 가지 전형적인 시스템, 즉 그람음성 대장균의 σ32(시그마32) 활성화 경로와 그람양성 유산균의 HrcA 억제 경로로 구분하고, 각각을 단순화된 미분방정식 모델로 구현하였다. 핵심은 두 시스템 모두 ‘자유형 샤프론(Chaperone)’이 전사인자의 활성을 조절한다는 점이다. σ32 시스템에서는 DnaK가 자유형일 때 σ32와 결합해 σ32의 활성을 억제하고, 열충격 시 단백질이 비접힘 상태가 증가하면서 자유 DnaK 농도가 감소, 결과적으로 σ32가 활성화되어 dnaK와 groEL 같은 샤프론 유전자를 전사한다. 반대로 HrcA 시스템에서는 HrcA가 자유형일 때 DNA에 결합해 억제 작용을 수행하고, GroE가 자유형이면 HrcA와 결합해 HrcA의 억제 활성을 차단한다. 열충격 시 비접힘 단백질이 늘어나 자유 GroE가 감소함에 따라 HrcA 억제가 해제되어 샤프론 유전자가 발현된다.
수학적 모델링에서는 각각의 전사인자·샤프론 복합체 형성에 대한 결합 상수(Kd)를 핵심 파라미터로 두었다. σ32‑DnaK 결합 상수는 실험적으로 100 nM 정도로 알려져 있으며, 모델 분석 결과 이 값이 낮을수록 시스템이 ‘자유 DnaK’ 농도의 미세 변화를 감지하는 감도 한계가 낮아져 과도한 잡음에 민감해진다. 따라서 σ32 시스템은 낮은 Kd(고친화도)에서 시작해 자유 DnaK 농도가 일정 수준 이하로 떨어질 때만 강한 피드백을 발동하도록 설계돼 있다.
반면 HrcA‑GroE 결합은 상대적으로 약한 친화도를 필요로 한다. 모델은 Kd가 마이크로몰 수준(≈1–10 µM)이어야 HrcA가 충분히 억제되지 않고, 열충격 시 자유 GroE 감소에 따라 HrcA 억제가 적절히 해제될 수 있음을 보여준다. 만약 결합이 너무 강하면 HrcA가 지속적으로 억제되어 열충격에 대한 동적 응답이 거의 일어나지 않는다. 따라서 두 시스템은 결합 친화도의 ‘하한’과 ‘상한’이 서로 반대 방향으로 설정돼야 함을 제시한다.
동적 시뮬레이션 결과는 두 회로가 전형적인 ‘빠른 상승‑느린 회복’ 패턴을 보이며, 열충격 후 샤프론 농도가 급격히 증가하고 이후 정상 수준으로 복귀한다는 점에서 거의 동일한 거동을 나타낸다. 이는 전사인자 조절 메커니즘이 다름에도 불구하고, 부정적 피드백 루프와 샤프론-전사인자 결합 특성이 시스템 전체의 동적 특성을 결정한다는 중요한 생물학적 원리를 뒷받침한다.
이 연구는 회로 수준에서의 설계 원칙이 미생물 스트레스 반응의 진화적 수렴을 설명할 수 있음을 보여준다. 또한, 합성생물학에서 열충격 회로를 재구성하거나 조절하려는 경우, 전사인자와 샤프론 사이의 결합 친화도를 목표값으로 설정함으로써 원하는 동적 특성을 정밀하게 튜닝할 수 있다는 실용적 시사점을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기