HIV 캡시드 단백질 결합에서 물 탈수 현상의 화학·지형 조절 메커니즘
초록
이 연구는 HIV 캡시드 단백질 C‑말단 도메인(CA‑C) 이합체 형성 과정에서 물 분자의 탈수 현상이 어떻게 일어나는지를 원자 수준 시뮬레이션으로 조사한다. 특수 샘플링 기법을 이용해 두 단백질 사이의 수분 밀도 분포를 측정한 결과, 야생형 단백질은 접촉 직전까지 물이 남아 있지만, 친수성 잔기를 비극성 잔기로 교체한 세 가지 돌연변이는 접촉 전 단계에서 탈수가 발생한다는 것을 확인했다. 탈수 현상은 교체된 잔기의 크기와 위치에 따라 수 나노미터 거리까지 협동적으로 영향을 미치며, 이는 기존의 ‘숨은 소수성 면적’만으로는 설명되지 않는 장거리 상호작용과 표면 토포그래피의 중요성을 강조한다.
상세 분석
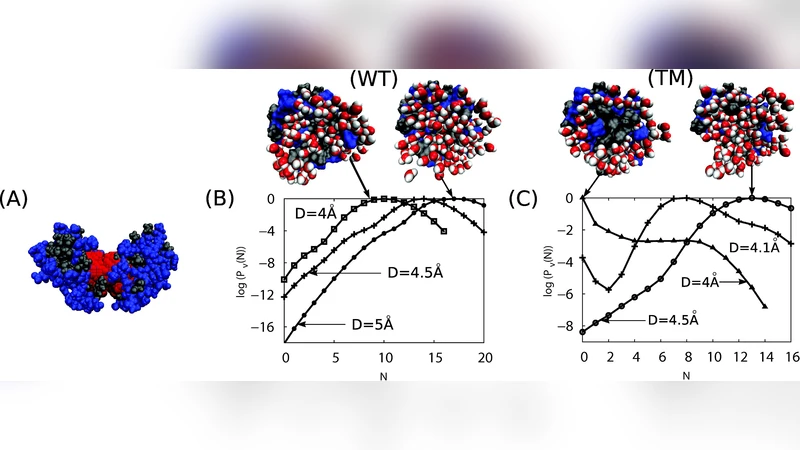
본 논문은 물‑단백질 계면이 건조 전이(drying transition) 근처에 존재한다는 최근 이론적 제안을, 실제 바이오 시스템인 HIV 캡시드 CA‑C 도메인 이합체에 적용해 검증한다. 저자들은 전통적인 분자동역학(MD) 시뮬레이션에 더해, 물의 국소 밀도 변화를 정밀하게 샘플링할 수 있는 INDUS(Indirect Umbrella Sampling)와 같은 특수 기법을 도입하였다. 두 CA‑C 단백질을 서로 접근시키면서, 중심축 거리(R)와 인터페이스 내 특정 아미노산 잔기의 종류·배열을 변수로 설정하고, 각 거리 단계에서 물의 평균 밀도와 분포 함수를 계산하였다.
시뮬레이션 결과, 야생형 CA‑C는 R ≈ 0.6 nm 이하에서만 물이 급격히 배제되는 ‘탈수’ 현상을 보였으며, 실제 접촉 전까지는 물이 완전히 남아 있었다. 이는 단백질 표면에 존재하는 여러 친수성 잔기(예: Asp, Glu, Lys)가 물과 강한 수소결합을 형성해 탈수를 억제한다는 것을 의미한다. 반면, 세 개의 친수성 잔기(D61, E62, K63)를 각각 비극성 알릴(Val) 혹은 페닐(Trp) 등으로 치환한 돌연변이 시뮬레이션에서는 R ≈ 0.8 nm에서부터 물이 급격히 감소하는 탈수 전이가 관찰되었다.
특히 주목할 점은, 이러한 탈수는 단일 잔기의 물리적 부피만을 고려한 것이 아니라, 치환된 잔기들의 공간적 배치와 표면 굴곡(topography)에 크게 의존한다는 것이다. 저자들은 동일한 부피를 갖는 작은 비극성 잔기(예: Ala)로 교체했을 때는 탈수가 일어나지 않으며, 반대로 큰 비극성 잔기(예: Phe)를 적절히 배치하면 탈수가 촉진된다는 것을 보여준다. 이는 물이 탈수될 때 필요한 ‘핵’이 되는 비극성 면적이 일정 크기 이상이어야 하며, 그 면적이 서로 멀리 떨어진 두 부위가 협동적으로 작용해 전체 인터페이스의 자유에너지 장벽을 낮춘다는 장거리 협동 효과를 시사한다.
또한, 물의 탈수 현상이 단백질‑단백질 결합 자유에너지에 미치는 정량적 영향을 평가하기 위해, 잠재적 평균 힘(potential of mean force, PMF)을 계산하였다. 탈수가 일어나는 돌연변이에서는 결합 자유에너지 장벽이 약 2–3 kcal·mol⁻¹ 낮아져, 결합 속도가 실험적으로 관찰된 것보다 크게 증가할 것으로 예측된다. 이는 물이 ‘중간 매개자’ 역할을 하면서 결합을 지연시키는 메커니즘을 물리적으로 설명한다.
결과적으로, 이 연구는 (1) 단백질 표면의 소수성·친수성 패턴이 물의 집합적 거동을 조절하고, (2) 물 탈수는 단백질‑단백질 결합의 초기 단계에서 결정적인 역할을 하며, (3) 표면 토포그래피와 잔기 크기의 미세 조정이 장거리 협동을 통해 탈수 전이를 유도할 수 있음을 입증한다. 이러한 통찰은 기존의 ‘숨은 소수성 면적(buried hydrophobic surface area)’만을 기준으로 한 결합 모델을 넘어, 물 매개 상호작용과 표면 구조를 동시에 고려한 새로운 설계 원칙을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기