단백질 결합에서 구조 변동과 잔기 구도 변화
초록
이 논문은 정상 모드 분석과 탄성 네트워크 모델을 이용해 단백질 잔기의 평형 진동을 정량화하고, 결합 전후의 측쇄 이등각 변화 통계를 수행한다. 잔기를 세 그룹(고변동, 중변동, 저변동)으로 분류하고, B‑factor와 비교해 용액 내 유연성을 더 정확히 반영함을 보인다. 또한 인터페이스 잔기의 약 20%가 로터머 전이를 겪으며, 나머지는 동일 로터머 내 미세 조정을 한다는 결과를 제시한다.
상세 분석
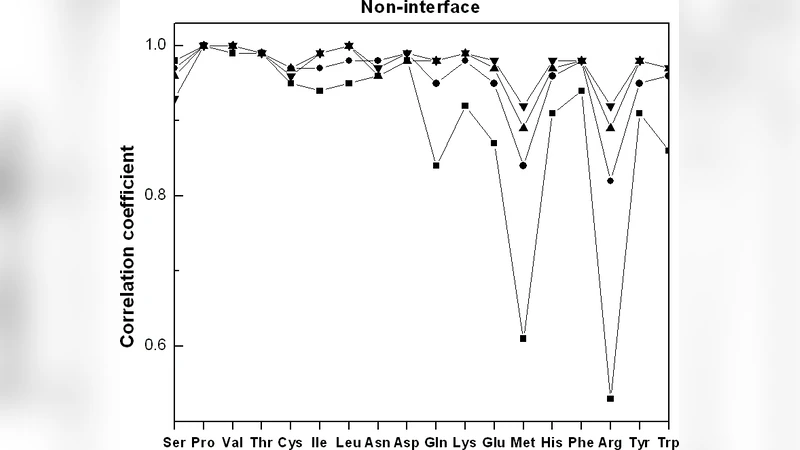
본 연구는 Vibe 프로그램으로 구현한 탄성 네트워크 모델을 사용해 184개의 비결합 단백질(92개 복합체)에서 잔기 중심질량의 평균 제곱 변동을 계산하고, 이를 전체 평균으로 정규화한 ‘모빌리티 비율’을 도출하였다. 이 비율을 기준으로 아미노산을 고변동(Gly, Ala, Ser, Pro, Asp), 중변동(Thr, Glu, Asn, Lys, Cys, Gln, Arg, Val), 저변동(His, Leu, Met, Ile, Tyr, Phe, Trp) 세 그룹으로 구분하였다. 고변동 잔기는 주로 루프와 무질서 영역에 풍부하고, 저변동 잔기는 알파‑헬릭스와 베타‑시트 같은 규칙적 2차 구조에 선호된다. 이는 단백질 열안정성에 대한 가설을 제시하는데, 고변동 잔기를 저변동 잔기로 치환하면 전반적 안정성이 향상될 수 있다. 또한 B‑factor와 비교했을 때, 용액 내 실제 유연성을 반영하는 모빌리티 비율이 변동 폭이 85%에 달해 더 민감함을 보여준다. 인터페이스와 비인터페이스 표면을 비교한 결과, Gly, Ala, Ser, Trp 등은 인터페이스에서 변동이 크게 감소했으며, 이는 비극성 잔기의 상호작용이 복합체 안정화에 기여함을 시사한다. 측쇄 이등각(χ1‑χ4) 분포는 입체 격자를 이용해 셀화했으며, 바인딩 전후의 확률 분포 상관계수를 계산하였다. 대부분의 아미노산은 격자 스텝이 커질수록 높은 상관을 보였으나, Met와 Arg는 인터페이스에서 상대적으로 낮은 상관을 보여 큰 회전 전이가 일어날 가능성을 나타낸다. 전체적으로 측쇄 회전 변화는 근위 이등각에서 원위 이등각으로 갈수록 증가했으며, 대칭성을 가진 잔기(Phe, Tyr, Asp, Glu)는 예외적으로 감소하는 경향을 보였다. 이러한 정량적 분석은 로터머 라이브러리 구축 및 결합 예측 알고리즘에 활용될 수 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기