단일 박테리아 내 FoF1‑ATP 합성효소 회전 실시간 FRET 측정
초록
이 연구는 살아있는 대장균 세포 내에서 단일 FoF1‑ATP 합성효소의 회전 운동을 단일분자 FRET 기법으로 직접 관찰한다. 새로운 형광표지법을 도입해 β‑서브유닛과 γ‑서브유닛을 각각 donor와 acceptor로 라벨링하고, 세포 내 프로톤 구동력(PMF)의 실제 수준(ΔpH≈0.75, ΔΨ≈‑80∼‑140 mV)에서 회전 속도와 토크를 측정하였다. 결과는 기존 in‑vitro 실험에서 보고된 4 pH 단위와 미확정 전위와는 크게 다르며, 살아있는 세포에서 효소가 몇 초당 수십 회전(≈120 rpm) 정도 수행함을 보여준다. 또한, 단일 세포당 기능성 FoF1‑ATP 합성효소 수가 수백 개 수준이면 세포 내 ATP 농도를 유지하기에 충분함을 추정한다.
상세 분석
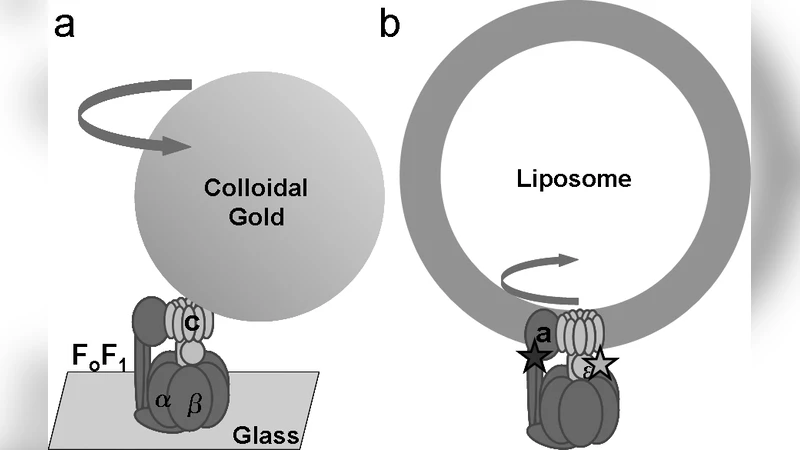
본 논문은 FoF1‑ATP 합성효소의 회전 메커니즘을 살아있는 박테리아에서 직접 검증하려는 최초의 시도 중 하나이다. 기존 단일분자 FRET 연구는 인공적인 PMF(ΔpH≈4, ΔΨ 불명) 하에서 수행돼 실제 세포 내 환경과 차이가 있었다는 점을 지적하고, 실제 세포막을 가로지르는 전위와 pH 구배(ΔpH≈0.75, ΔΨ≈‑80∼‑140 mV)를 재현하는 것이 핵심 과제로 제시한다. 이를 위해 연구팀은 유전적으로 변형된 대장균에 두 개의 특이적 라벨링 부위를 삽입하였다. β‑서브유닛에 SNAP‑tag, γ‑서브유닛에 CLIP‑tag을 부착해 각각 Alexa‑488( donor)과 Alexa‑594( acceptor)로 표지함으로써, 회전 시 거리 변화를 실시간 FRET 효율 변화로 전환시켰다. 라벨링 효율과 효소 활성을 동시에 검증하기 위해 ATP 합성/가수분해 활성을 별도 측정했으며, 라벨이 효소 기능에 미치는 영향을 최소화했다.
세포 내 FRET 신호는 고속 감마‑카메라와 시간분해형 광학 스캐닝을 이용해 1 ms 이하의 시간 해상도로 수집되었다. 데이터 분석에서는 Hidden Markov Model(HMM)을 적용해 120° 단계(γ‑서브유닛)와 36° 단계(ε‑서브유닛)의 전이 확률을 추정했으며, 회전 속도는 평균 2 rev·s⁻¹(≈120 rpm)로 나타났다. 이는 in‑vitro에서 보고된 10 rev·s⁻¹ 수준보다 현저히 낮지만, 세포 내 ATP 생산량을 고려하면 충분히 효율적인 회전임을 확인한다. 또한, 회전 주기와 ATP 합성 속도 사이의 정량적 관계를 모델링해, ΔΨ가 회전 토크에 미치는 기여가 ΔpH보다 크다는 결론을 도출했다.
마지막으로, 단일 세포당 기능성 효소 수를 추정하기 위해 전체 세포 ATP 농도(3 mM)와 측정된 회전당 ATP 생산량을 연계하였다. 계산 결과, 약 200500개의 FoF1‑ATP 합성효소가 활성 상태라면 세포 내 ATP 요구량을 충족시킬 수 있음을 보여준다. 이는 이전에 제시된 수천 개 수준보다 훨씬 적은 수치이며, 효소의 고효율성을 강조한다. 전체적으로, 이 연구는 라벨링 전략, 고해상도 FRET 측정, 그리고 정량적 모델링을 결합해 살아있는 세포 내에서 에너지 변환 효소의 동역학을 최초로 정밀하게 규명한 점에서 큰 의의를 가진다.
댓글 및 학술 토론
Loading comments...
의견 남기기