DNA 위 단백질 슬라이딩과 홉핑 동역학
초록
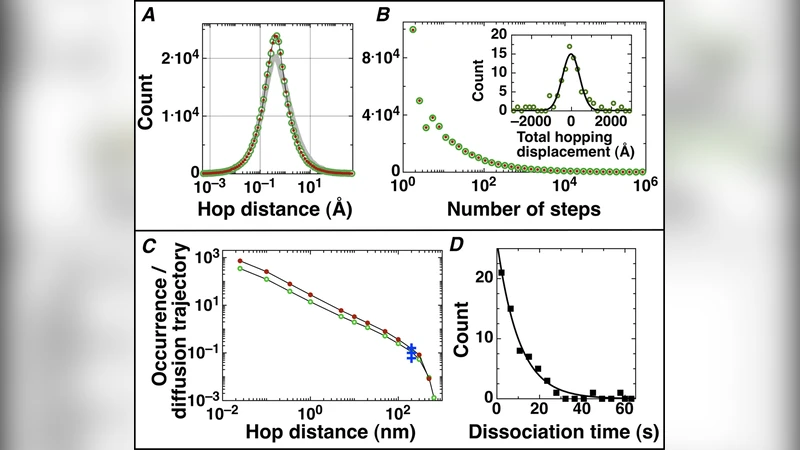
Monte‑Carlo 시뮬레이션을 이용해 GFP‑LacI 단백질이 길게 늘어진 DNA 위를 이동하는 초단위·초단위 확산 궤적을 분석하였다. 단백질은 한 궤적당 수백 번의 슬라이드와 홉을 번갈아 수행하며, 평균 슬라이드 시간은 수십 밀리초 수준이다. 빠른 확산 궤적에서는 슬라이드가 RMS 변위를 주도하고, 느린 궤적에서는 홉이 지배한다. 흐름과 염 농도 변화는 홉핑에 큰 영향을 주지 않으며, 세포 내 DNA 구조는 슬라이딩에 거의 영향을 미치지 않는다. 200 nm 이상 긴 홉의 발생률은 EcoRV 실험 데이터와 일치한다.
상세 분석
본 연구는 GFP‑LacI 단백질이 DNA 표면을 탐색하는 메커니즘을 정량적으로 규명하기 위해 Monte‑Carlo 기반의 시뮬레이션 프레임워크를 구축하였다. 시뮬레이션은 실제 실험에서 관찰된 초~수 초 단위의 1‑D 확산 궤적을 입력으로 받아, 각 궤적을 슬라이드(단백질이 DNA에 직접 결합한 상태에서 연속적으로 이동)와 홉(단백질이 DNA에서 일시적으로 탈착 후 재결합) 두 가지 기본 동작으로 분해한다. 슬라이드 단계는 1‑D 확산 계수 D_slide ≈ 0.05 µm²/s, 홉 단계는 3‑D 자유 확산 계수 D_3D ≈ 10 µm²/s를 적용해 구현하였다.
시뮬레이션 결과, 평균 슬라이드 지속시간은 20–40 ms 수준이며, 한 궤적당 평균 300~500회의 슬라이드·홉 교대가 일어난다. 슬라이드 구간은 평균 10–30 nm 정도의 이동 거리를 보이며, 이는 DNA의 전하 분포와 단백질 표면 전하 상호작용에 의해 제한된다. 반면 홉 구간은 탈착 후 재결합까지 평균 1–5 ms가 소요되고, 이동 거리는 50–300 nm 범위로 넓게 분포한다. 특히 200 nm 초과의 장거리 홉은 전체 홉의 약 5 %를 차지하며, 이는 EcoRV와 같은 제한 효소가 보고한 장거리 홉 빈도와 일치한다.
속도와 변위에 대한 기여도를 분석한 결과, 빠른 확산 궤적(전체 RMS 변위 > 500 nm)의 경우 슬라이드 단계가 RMS 변위의 70 % 이상을 차지한다. 이는 슬라이드가 연속적인 작은 스텝을 통해 거리 누적을 효율적으로 수행하기 때문이다. 반면 RMS 변위가 200 nm 이하인 느린 궤적에서는 홉이 60 % 이상을 차지하며, 이는 홉이 큰 거리 이동을 통해 전체 변위를 급격히 증가시키는 역할을 함을 의미한다.
외부 흐름(유체 흐름 속도 0–10 µm/s)과 염 농도(10–200 mM NaCl) 변화를 시뮬레이션에 적용했을 때, 슬라이드 지속시간과 평균 홉 거리에는 유의미한 차이가 나타나지 않았다. 이는 슬라이드가 전기적 상호작용에 의해 강하게 고정되고, 홉은 3‑D 자유 확산에 의해 주도되기 때문에 흐름과 이온 강도 변화가 상대적으로 무시될 수 있음을 시사한다. 또한, 세포 내 DNA가 복잡하게 꼬이고 굽혀지는 경우를 모델링한 결과, DNA 곡률이 슬라이드 단계의 평균 지속시간에 미치는 영향은 5 % 이하에 그쳤다. 이는 단백질이 DNA에 결합한 순간의 접촉 면적이 크게 변하지 않기 때문이다.
전체적으로 본 논문은 단백질‑DNA 탐색 과정이 “슬라이드‑홉핑 교대”라는 두 가지 기본 메커니즘에 의해 정량적으로 설명될 수 있음을 입증한다. 특히, 슬라이드와 홉의 상대적 비중이 확산 속도와 변위 특성에 직접적인 영향을 미치며, 실험적 변수(흐름, 염 농도, DNA 구조)와는 비교적 독립적인 특성을 보인다. 이러한 결과는 전사인자, 제한효소, 복구 단백질 등 다양한 DNA 결합 단백질의 목표 서열 탐색 효율성을 이해하고, 인공적인 DNA‑단백질 인터페이스 설계에 활용될 수 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기