바이러스 캡시드 자기조립 모델링과 설계 분석
초록
본 논문은 저해상도 입자 모델을 이용해 구형 바이러스 캡시드의 자기조립 과정을 분자동역학(MD) 시뮬레이션으로 조사한다. 60‑입자(T=1)와 180‑입자(T=3) 껍질을 대상으로, 가역·비가역 결합 방식과 명시적 용매 포함 여부를 바꾸어 실험하였다. 결과는 조립이 고도로 가역적인 단계들의 연쇄로 진행되며, 중간체는 강하게 결합된 소수의 형태만이 실제로 관찰된다는 점을 보여준다.
상세 분석
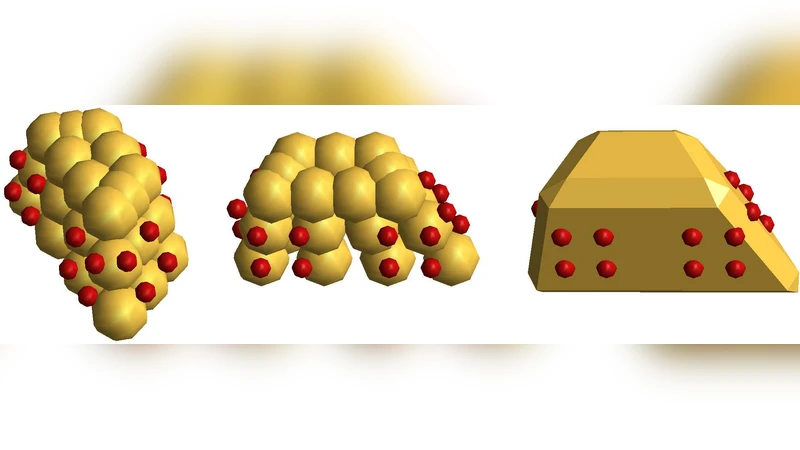
이 연구는 바이러스 캡시드 자기조립을 이해하기 위해 ‘단순화된 저해상도 모델’이라는 전략을 채택하였다. 입자는 강체 형태의 소프트 구(soft‑sphere) 어셈블리로 구성되며, 각 입자는 3~5개의 끌어당김 사이트(attraction site)를 갖는다. 끌어당김 사이트 간 상호작용은 역전력(inverse‑power) 포텐셜과 근거리에서의 조화탄성 포텐셜을 결합한 형태로 정의되어, 입자가 올바른 각도와 위치에 결합했을 때 최소 에너지를 제공한다. 비가역 결합에서는 결합이 형성되면 영구히 유지되도록 제약을 두어 계산 비용을 절감했으며, 가역 결합에서는 결합·해리 전이가 자유롭게 일어나도록 하여 실제 물리적 상황을 모사하였다.
시뮬레이션은 크게 두 가지 껍질 크기, 즉 60개의 삼각형 입자로 이루어진 T=1 icosahedral 껍질과 180개의 사다리꼴 입자로 구성된 T=3 껍질을 대상으로 수행되었다. T=3 구조에서는 ‘준동등성(quasi‑equivalence)’ 개념을 적용해 입자 종류를 B, G, R 세 가지 색으로 구분하고, 각 색에 따라 결합 각도가 미세하게 달라지도록 설계함으로써 실제 바이러스 캡시드가 보이는 비대칭성을 재현하였다.
용매를 명시적으로 포함한 경우, 물 분자는 입자들의 운동을 완화하고, 결합 과정에서 발생하는 발열을 흡수하는 열욕조 역할을 수행한다. 이는 입자 간 직접 충돌 없이도 클러스터가 분리·재결합할 수 있게 하여, 가역적인 조립 단계가 더욱 원활히 진행되도록 돕는다. 용매가 없는 경우에는 입자들의 운동이 ‘탄성 충돌(billiard‑like)’ 형태를 띠어, 비가역 결합 시에도 조립 효율이 크게 저하되지 않도록 초기 단계에서 강제적인 결합 제한을 두었다.
시뮬레이션 결과는 두드러진 몇 가지 특징을 보여준다. 첫째, 효율적인 조립은 ‘고도로 가역적인 단계들의 연쇄(cascade of reversible stages)’를 통해 이루어진다. 초기에는 작은 트리머(trimer)·다이머(dimer) 형태가 빠르게 형성되고, 이들이 다시 결합·해리하면서 최적의 구조로 재배열된다. 둘째, 가능한 중간체 조합은 이론적으로 매우 다양하지만, 실제로 관찰되는 중간체는 에너지적으로 가장 안정한 소수의 결합 형태에 국한된다. 이는 시스템이 낮은 자유에너지 경로를 선호하고, 비정상적인 결함이 발생하면 즉시 해리되어 다시 시도하기 때문으로 해석된다. 셋째, 가역 결합을 허용했을 때 최종 완전 껍질의 수율이 비가역 결합보다 현저히 높았다. 비가역 모델에서는 초기 잘못된 결합이 영구히 남아 조립 실패를 초래했지만, 가역 모델에서는 이러한 오류가 스스로 교정된다.
또한, 입자 설계에 있어서 ‘입자 두께(thickness)’와 ‘끌어당김 사이트의 위치’가 조립 성공률에 큰 영향을 미친다. 두께를 늘려 입자 간 비의도적 결합을 물리적으로 차단하고, 사이트를 입체적으로 배치함으로써 올바른 면 맞대기가 보장되었다. 이는 실제 캡시드 단백질이 복잡한 3차원 구조를 가지는 이유와 일맥상통한다.
전반적으로 이 논문은 저해상도 입자 모델이 복잡한 바이러스 캡시드 자기조립 현상을 정량적으로 재현할 수 있음을 입증하고, 가역성, 용매 효과, 입자 기하학적 설계가 조립 효율에 미치는 영향을 체계적으로 분석하였다. 이러한 결과는 향후 나노스케일 자가조립 시스템 설계와 항바이러스 전략 개발에 중요한 이론적 기반을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기