단백질‑단백질 만남에 대한 이방성의 역할
초록
이 연구는 타원형 입자와 구형 결합 부위를 모델링하여, 단백질의 형태 이방성이 만남 속도에 미치는 영향을 정량화한다. 시뮬레이션 결과, 종횡비에 따른 스테릭 효과가 주된 요인이며, 이방성 확산은 상대적으로 미미한 영향을 미친다. 또한, 이방성 확산이 등방성으로 전환되는 시간은 실제 단백질 만남 시간보다 훨씬 짧아 실험적 상황에서 무시할 수 있음을 보여준다.
상세 분석
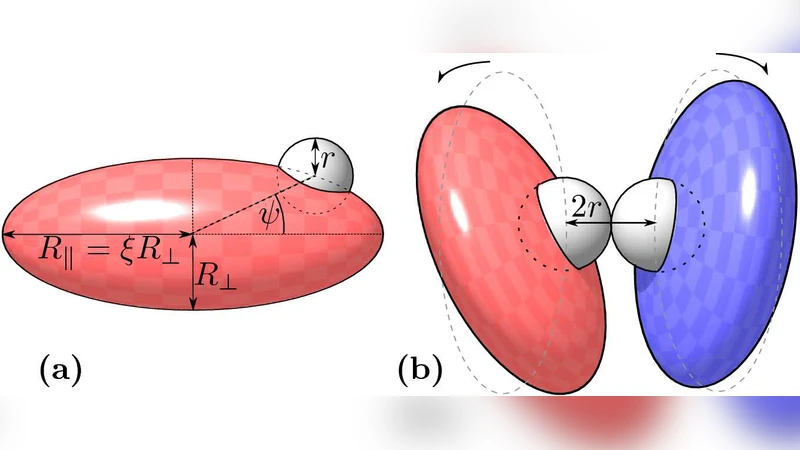
본 논문은 단백질‑단백질 상호작용을 두 단계, 즉 확산에 의한 운반 단계와 실제 결합 반응 단계로 구분하고, 특히 운반 단계에서 입자의 기하학적 이방성이 어떻게 작용하는지를 탐구한다. 연구자는 타원형(ellipsoidal) 입자를 기본 형태로 채택하고, 그 표면에 구형( spherical) ‘encounter patch’를 배치함으로써 실제 단백질 표면의 비대칭성과 결합 부위의 국소성을 동시에 모델링하였다. 종횡비 ξ(가장 긴 축과 가장 짧은 축의 비) 를 변화시켜 다양한 이방성을 구현하고, Brownian dynamics 시뮬레이션을 통해 수천 개의 독립적인 만남 시나리오를 수행하였다.
시뮬레이션 결과는 두 가지 주요 메커니즘을 구분한다. 첫 번째는 스테릭(steric) 효과이다. 종횡비가 커질수록 입자의 부피는 일정하게 유지되지만, 장축 방향으로 길어지면서 결합 부위가 다른 입자와 충돌하기 전까지 접근 가능한 공간이 제한된다. 이는 실제 단백질이 비구형 구조를 가질 때, 결합 부위가 ‘숨겨지는’ 현상과 일맥상통한다. 두 번째는 이방성 확산이다. 타원형 입자는 회전 및 전이 확산 계수가 방향에 따라 다르며, 이는 초기 접촉 확률에 영향을 줄 것으로 예상된다. 그러나 저자들은 분석적 계산을 통해 이방성 확산이 등방성 확산으로 전환되는 전이 시간 τ가 수십 나노초 수준이며, 일반적인 단백질 만남 시간(마이크로초~밀리초)보다 현저히 짧다는 것을 입증하였다. 따라서 실질적인 만남 과정에서는 확산이 이미 등방성으로 작동하고 있기에, 이방성 확산 자체가 전체 만남 속도 k에 미치는 기여는 미미하다.
이러한 결과는 기존의 단순 구형 모델이 실제 단백질 상호작용을 설명하는 데 충분히 근접했음을 시사한다. 다만, 스테릭 효과는 종횡비에 따라 k가 크게 변동함을 보여주므로, 구조적 이방성을 고려한 설계(예: 약물 설계 시 타깃 단백질의 비대칭 부위 활용)에서는 반드시 반영해야 한다. 또한, 전이 시간 τ의 정량적 추정은 실험적 단백질‑단백질 결합 속도 측정과 비교하여 모델의 신뢰성을 검증하는 데 유용한 기준이 될 수 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기