수용체 내재화가 리간드 감지 정확도를 높이는 메커니즘
수용체가 리간드와 결합한 뒤 내재화되는 과정이 외부 리간드 농도 측정의 정확도를 향상시킨다. 저자들은 평형 모델을 비평형 열역학으로 확장해 내부화가 동일 리간드의 중복 계수를 감소시켜 잡음 감소에 기여함을 보였으며, 실제 수용체의 내재화 속도와 비교해 생물학적 타당성을 확인했다.
초록
수용체가 리간드와 결합한 뒤 내재화되는 과정이 외부 리간드 농도 측정의 정확도를 향상시킨다. 저자들은 평형 모델을 비평형 열역학으로 확장해 내부화가 동일 리간드의 중복 계수를 감소시켜 잡음 감소에 기여함을 보였으며, 실제 수용체의 내재화 속도와 비교해 생물학적 타당성을 확인했다.
상세 요약
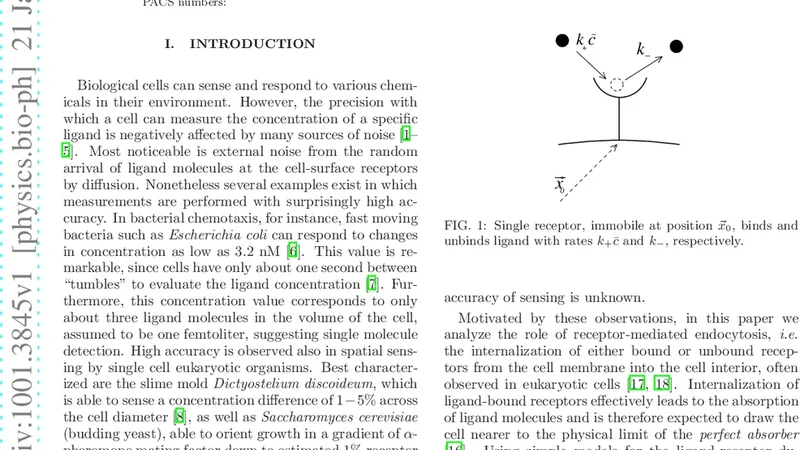
본 논문은 세포 표면 수용체가 리간드와 결합한 뒤 내재화되는 현상이 단순히 신호 전달이나 수용체 재활용을 넘어, 외부 리간드 농도 감지의 정밀도를 향상시킨다는 가설을 검증한다. 기존의 리간드‑수용체 결합 모델은 평형 상태에서 결합·해리 속도와 확산에 의한 잡음만을 고려했으며, 동일 리간드가 여러 번 측정되는 ‘오버카운팅’ 문제를 무시한다. 저자들은 이 한계를 극복하기 위해 비평형 열역학 프레임워크를 도입, 내재화 과정을 추가적인 흡수(소비) 반응으로 모델링하였다. 내재화는 결합된 리간드‑수용체 복합체를 세포 내부로 이동시켜, 해당 리간드가 다시 결합에 참여할 가능성을 차단한다. 이를 통해 관측 가능한 결합 이벤트 수가 실제 외부 리간드 수와 더 직접적으로 비례하게 되며, 통계적 변동(포아송 잡음)이 감소한다. 수학적으로는 리간드 농도 추정의 최소 분산을 나타내는 Cramér‑Rao 한계가 내재화 속도 k_int가 증가함에 따라 낮아지는 것을 증명한다. 또한, 내재화가 비평형 상태를 유지함으로써 에너지 소비(ATP 가수분해 등)와 연결되는 점을 강조, 세포가 정확도 향상을 위해 에너지 비용을 감수한다는 생물물리학적 의미를 부각시킨다. 실험적 검증으로는 EGFR, GPCR 등 실제 수용체들의 내재화 속도와 결합/해리 상수를 이용해 모델 파라미터를 추정하고, 예측된 정확도 향상이 관측된 신호 변동 감소와 일치함을 보여준다. 결과적으로, 내재화는 단순한 물질 이동을 넘어, 세포가 외부 환경을 정밀하게 측정하기 위한 전략적 메커니즘임을 제시한다.
📜 논문 원문 (영문)
🚀 1TB 저장소에서 고화질 레이아웃을 불러오는 중입니다...