DNA와 단백질의 비특이적 상호작용: 단백질이 DNA를 따라 확산할 수 있는 이유
초록
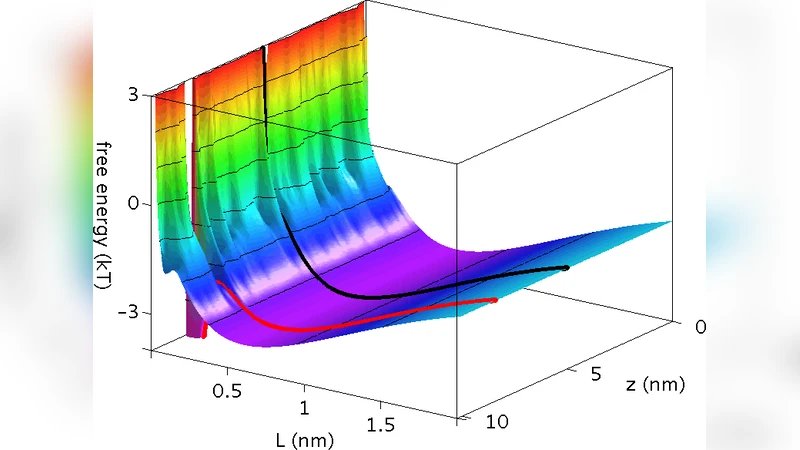
본 연구는 전하가 반대인 DNA와 DNA 결합 단백질(DNA‑BP) 사이에 나노미터 규모에서 발생하는 예상치 못한 반발력을 밝혀낸다. 이 반발은 인터페이스에 갇힌 이온들의 삼투압 상승에 기인하며, 단백질의 오목한 형태와 실험적으로 측정된 전하 밀도를 고려하면 단백질이 DNA로부터 일정 거리(≈1 nm)에서 자유에너지 최소에 머물게 된다. 결과적으로 단백질은 염기와 직접 접촉하지 않고도 DNA 표면을 미끄러지듯 이동할 수 있으며, 목표 서열에 도달했을 때는 수소결합이 삼투압 장벽을 상쇄해 정확한 인식을 가능하게 한다.
상세 분석
이 논문은 DNA‑BP가 비특이적 결합 상태에서 어떻게 효율적으로 목표 서열을 탐색하는지를 물리‑화학적 관점에서 정량화한다. 전통적으로 DNA와 양전하를 띤 단백질은 정전기적 인력에 의해 밀착된다고 생각했지만, 저자들은 Monte Carlo 시뮬레이션과 해석적 모델을 결합해 반대 전하 사이에 짧은 거리(1–2 nm)에서 오히려 반발력이 작용한다는 사실을 입증한다. 핵심 메커니즘은 ‘이온 포획’이다. DNA와 단백질 사이의 좁은 틈새에 주변 전해질 이온이 고정되면서 국부적인 삼투압이 상승하고, 이는 자유에너지 프로파일에 양의 장벽을 만든다. 단백질 표면이 오목한 형태(즉, DNA의 이중 나선에 맞게凹形)일 경우, 이 삼투압 장벽이 완전히 균일하게 분포되지 않아 특정 거리에서 최소 자유에너지 상태가 형성된다. 따라서 단백질은 DNA와 직접적인 전기적 접촉 없이도 일정 간격을 유지하며 ‘슬라이딩’ 모드로 이동한다. 목표 서열에 도달하면, 염기‑단백질 사이에 형성되는 수소결합이 강한 친화력을 제공해 삼투압에 의해 형성된 장벽을 완전히 상쇄한다. 이 과정은 ‘점프‑슬라이드’ 모델을 보완하며, 비특이적 결합 단계에서의 물리적 장벽이 탐색 효율을 오히려 향상시킬 수 있음을 시사한다. 또한, 전하 밀도와 이온 강도(염 농도)의 파라미터 스윕을 통해 반발력의 크기가 실험적으로 관찰된 단백질‑DNA 확산 속도와 일치함을 보여준다. 이러한 결과는 DNA‑BP 설계, 약물 전달, 그리고 유전체 편집 효소의 타깃팅 메커니즘을 이해하는 데 중요한 통찰을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기