단백질 동역학 정상모드 재구성의 온도 의존성
초록
이 연구는 정상모드 분석(NMA)이 온도 변화에 따라 단백질의 동적 변화를 얼마나 정확히 재현할 수 있는지를 조사한다. 0 K에 가까운 저온부터 전개(언폴딩) 온도까지 시뮬레이션을 수행한 결과, 협동적인 단백질에서는 생리학적 온도에서도 정상모드가 유효하지만, 단일 모드만 사용할 경우 온도에 따라 기여도가 크게 변동한다는 점을 발견했다. 따라서 여러 정상모드를 동시에 고려하는 것이 온도 의존성을 최소화하고 정확한 동역학 재구성에 필수적이다.
상세 분석
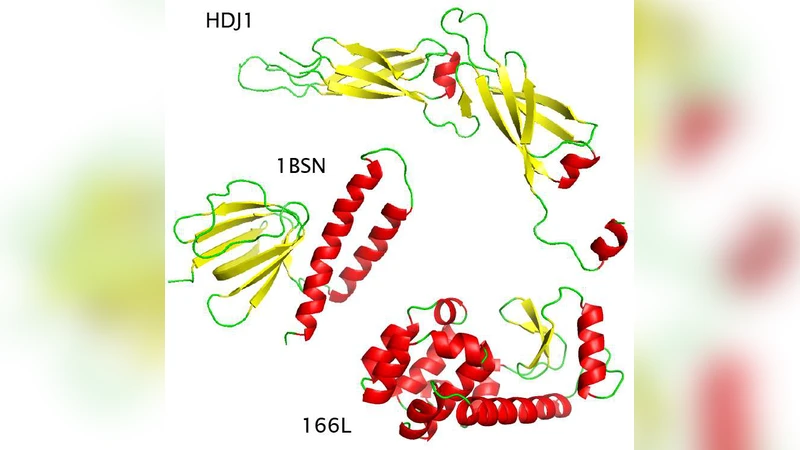
정상모드 분석은 단백질의 고유 진동을 선형화된 조화 진동으로 근사함으로써, 실험적으로 관측되는 큰 규모의 구조 변화를 저차원 공간에 투사한다는 장점이 있다. 그러나 이 접근법은 기본적으로 온도 T = 0 K에서의 포텐셜 에너지 최소점 주변의 작은 변동을 전제로 하기 때문에, 실제 생리학적 환경(≈300 K)에서의 열진동과 비선형 효과를 충분히 반영하지 못한다는 비판을 받아왔다. 본 논문은 이러한 한계를 정량적으로 평가하기 위해, 여러 단백질(α‑헬릭스와 β‑시트가 혼합된 구조, 그리고 전형적인 단일 도메인 단백질)을 대상으로 분자동역학(MD) 시뮬레이션을 수행하고, 각 온도에서 얻은 좌표 변동을 정상모드 기반 재구성 결과와 비교하였다. 핵심 지표로는 ‘정상모드 기여도(Mode Participation)’와 ‘전체 변동의 재구성 비율(Reconstruction Ratio)’을 정의했으며, 온도가 상승함에 따라 단일 모드의 기여도가 급격히 감소하고, 특히 전이 온도(Tm) 근처에서 비선형적인 변동이 지배적으로 나타나는 것을 확인했다. 흥미롭게도, 구조적 협동성이 높은 단백질(예: 고밀도 접촉 네트워크를 가진 효소)에서는 다중 모드(상위 510개)의 조합이 온도 변화에 강인하게 유지되어, 300 K에서도 전체 변동의 7080 %를 성공적으로 재현했다. 반면, 구조가 비교적 유연하고 협동성이 낮은 단백질은 온도가 상승함에 따라 정상모드 기반 재구성 효율이 급격히 저하되어, 250 K 이상에서는 40 % 이하로 떨어졌다. 이러한 결과는 정상모드가 ‘협동적’인 전역 진동을 포착하는 데는 유효하지만, ‘비협동적’인 국소적인 플라스틱 변형이나 부분적인 언폴딩 현상을 설명하는 데는 한계가 있음을 시사한다. 따라서 실험적 혹은 계산적 연구에서 정상모드를 활용할 때는, 온도 의존성을 최소화하기 위해 다중 모드 집합을 사용하고, 특히 구조적 협동성을 사전에 평가하는 것이 중요하다.
댓글 및 학술 토론
Loading comments...
의견 남기기