전기구조와 쌍극자 모멘트가 밝혀낸 차리보톡신의 칼륨 채널 차단 메커니즘
초록
본 연구는 양자역학 계산을 통해 스콜피온 독소인 차리보톡신(ChTX)의 전자구조와 쌍극자 모멘트를 분석하였다. ChTX는 145 D의 큰 쌍극자 모멘트를 가지고 있으며, 이는 KcsA 칼륨 채널의 403 D 매크로쌍극자에 의해 회전되어 세포 표면에서 올바른 방향으로 정렬된다. 전자 궤도 분석 결과, HOMO는 Trp14에, LUMO·LUMO+1·LUMO+2는 세 개의 이황화 결합에 국한된다. Trp14를 알라닌으로 치환하면 HOMO‑LUMO 에너지 간격을 효과적으로 조절할 수 있으며, 이황화 결합을 L‑α‑아미노부티르산 두 개로 대체해도 간격은 변하지 않는다.
상세 분석
본 논문은 전통적인 실험적 접근이 어려운 펩타이드‑이온채널 상호작용을 전자구조 수준에서 해석하기 위해, 밀도범함수이론(DFT) 기반 양자역학 시뮬레이션을 적용하였다. 먼저, 차리보톡신(ChTX)의 37개의 아미노산 서열과 3개의 이황화 결합을 포함한 전체 구조를 최적화하고, 전하 분포와 전기적 쌍극자 모멘트를 정밀히 계산하였다. 결과적으로 ChTX는 145 D라는 매우 큰 쌍극자 모멘트를 나타내었으며, 이는 주변 환경, 특히 KcsA와 같은 대형 이온채널이 생성하는 403 D 매크로쌍극자와 상호작용할 때 회전 토크를 발생시켜 펩타이드가 채널 입구에 최적의 방향으로 접근하도록 돕는다. 이러한 전기적 정렬 메커니즘은 기존에 제시된 ‘전하 상보성’ 가설을 전자구조 수준에서 실증한다는 점에서 의미가 크다.
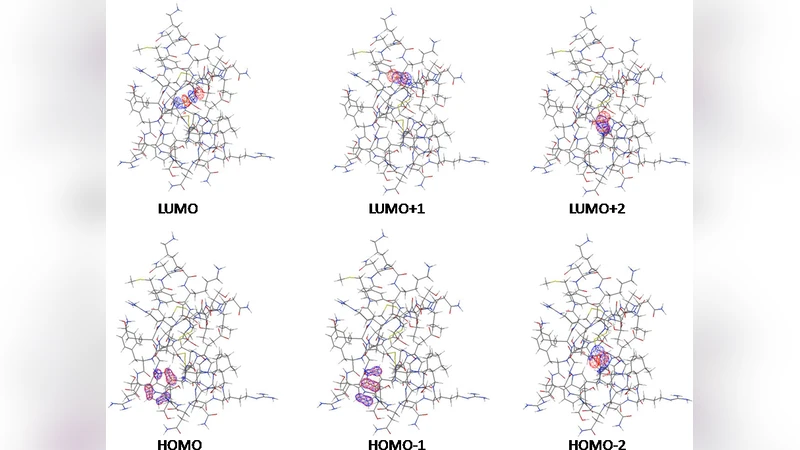
전자 궤도 분석에서는 최상위 점유 궤도(HOMO)가 Trp14 잔기에 국한되는 것을 확인하였다. Trp14는 큰 π 전자 구름을 가지고 있어 전자밀도가 집중되는 부위이며, 이는 전자 전달 및 광학적 특성에 직접적인 영향을 미친다. 반면, 최저 비점유 궤도(LUMO, LUMO+1, LUMO+2)는 각각 세 개의 이황화 결합(S‑S) 근처에 위치한다. 이황화 결합은 전자 친화도가 높아 전자 수용체 역할을 수행하므로, ChTX의 전자 수용성 및 반응성을 결정짓는 핵심 부위로 작용한다.
논문은 또한 HOMO‑LUMO 에너지 간격(H‑L gap)을 조절하는 두 가지 전략을 제시한다. 첫 번째는 Trp14를 알라닌(Ala14)으로 치환하는 것으로, 큰 π 시스템을 제거함으로써 HOMO 에너지 레벨을 낮추어 H‑L gap을 확대한다. 두 번째는 LUMO와 연관된 이황화 결합을 제거하고, 대신 L‑α‑아미노부티르산(α‑Abu) 두 개를 삽입하는 방법이다. 흥미롭게도, 이 변형은 LUMO 에너지에 큰 변화를 일으키지 않아 H‑L gap이 거의 유지된다. 이러한 결과는 펩타이드의 전자적 특성을 목표로 설계할 때, 특정 잔기의 교체가 구조적 안정성을 크게 해치지 않으면서도 전자적 파라미터를 미세 조정할 수 있음을 시사한다.
전반적으로, 본 연구는 전자구조와 전기적 쌍극자 모멘트가 펩타이드‑채널 상호작용에 미치는 영향을 정량적으로 규명함으로써, 향후 스콜피온 독소 기반의 약물 설계 및 전기생물학적 모델링에 중요한 이론적 토대를 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기