수동 큐레이션 데이터베이스와 예측 알고리즘을 활용한 생물학적 불린 네트워크 구축
초록
본 논문은 전사체·단백질 상호작용 데이터베이스와 RNAi 스크리닝 결과를 결합해, 관심 단백질 집합의 서브네트워크를 자동으로 추출하고 신호 흐름 및 활성·억제 관계를 예측한다. 이를 기반으로 불린 네트워크를 생성하여 정적 상태와 자극 반응을 모델링한다.
상세 분석
이 연구는 현재 생물학적 네트워크 모델링 분야에서 가장 큰 과제 중 하나인 ‘데이터 통합과 자동화’를 해결하고자 한다. 먼저, 저자들은 STRING, BioGRID, IntAct 등 다수의 공개 PPI(Protein‑Protein Interaction) 데이터베이스를 수동으로 큐레이션하여 신뢰도 높은 상호작용 집합을 구축한다. 여기서 ‘수동 큐레이션’은 자동화된 스크리닝만으로는 잡히지 않는 실험적 검증 정보와 문헌 기반 증거를 보강함으로써, 가짜 양성(false positive)을 최소화한다는 점에서 의미가 크다.
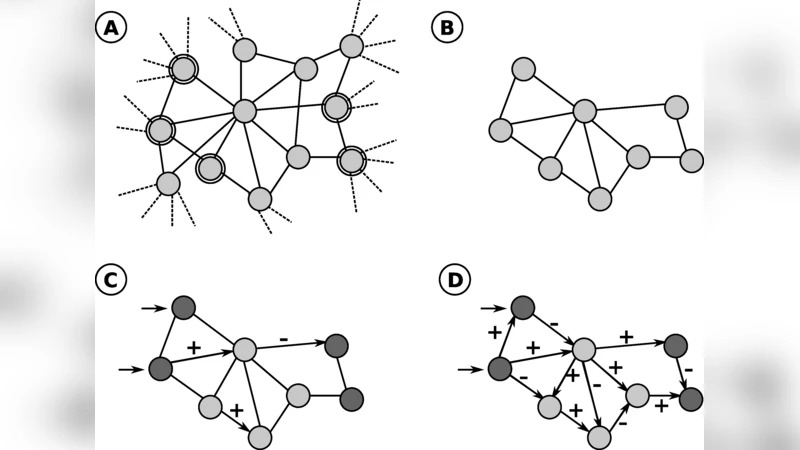
다음 단계에서는 그래프 이론 기반 알고리즘, 예를 들어 최소 스패닝 트리(MST)와 커뮤니티 탐지 기법을 적용해 전역 인터액톰에서 관심 단백질군에 대한 최적 서브네트워크를 추출한다. 이때 ‘관련성 점수’를 정의해, 직접적인 물리적 결합뿐 아니라 기능적 연관성까지 고려한다.
신호 흐름 방향성 예측은 베이지안 네트워크 혹은 퍼지 로직 기반의 방향성 추정 모델을 활용한다. 저자들은 기존에 알려진 신호 전달 경로(예: MAPK, PI3K‑AKT)를 학습 데이터로 사용해, 새로운 연결에 대한 방향성을 확률적으로 할당한다. 활성·억제 효과는 대규모 RNAi 스크리닝 결과와 연계하여, 특정 유전자의 억제가 하위 단백질의 발현에 미치는 영향을 정량화한다. 이를 통해 각 엣지에 ‘+’(활성) 혹은 ‘‑’(억제) 라벨을 부여한다.
이러한 정보를 바탕으로 Boolean 모델을 자동 생성한다. 각 노드는 ‘ON/OFF’ 상태를 가지며, 논리 함수를 통해 입력 노드들의 조합에 따라 출력이 결정된다. 저자들은 GINsim, BoolNet 등 기존 Boolean 시뮬레이터와 연동해, 네트워크의 고정점(steady state)과 시뮬레이션된 자극(예: 성장인자, 스트레스) 반응을 탐색한다. 결과적으로, 실험적으로 검증된 몇몇 경로는 모델이 정확히 재현했으며, 새로운 가설적 회로도 도출되었다.
핵심적인 기여는 (1) 수동 큐레이션과 자동 알고리즘을 결합해 데이터 품질을 확보하면서도 대규모 네트워크를 효율적으로 추출, (2) 방향성 및 활성·억제 라벨을 정량적으로 예측해 Boolean 모델에 바로 적용, (3) 자동화된 파이프라인을 통해 연구자가 별도 코딩 없이도 동적 시스템 분석을 수행할 수 있게 한 점이다. 이러한 접근은 시스템 생물학, 약물 타깃 탐색, 그리고 맞춤형 치료 전략 수립에 유용하게 활용될 수 있다.
댓글 및 학술 토론
Loading comments...
의견 남기기