거대분자 혼탁과 일시적 미세소관 결합 단백질이 키네신 모터 수송에 미치는 영향
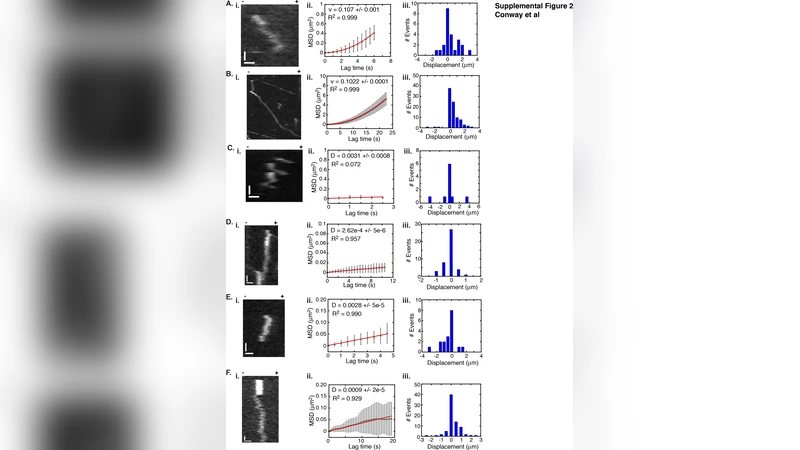
초록
이 연구는 세포 내 복잡하고 혼잡한 환경을 모사하기 위해 관능성 없는 고분자와 일시적으로 결합하는 미세소관 결합 단백질(MAP)을 이용해 단일 키네신‑1 모터의 이동을 in vitro에서 재구성하였다. 고분자 혼탁은 키네신의 이동 거리(run length)를 증가시켰지만, 비특이적 결합과 확산 현상을 촉진하였다. 반면, 일시적 MAP은 전진 속도를 감소시켰지만 결합 지속 시간에는 큰 영향을 주지 않아, 안정적으로 결합하는 tau와는 다른 장애물 효과를 보였다.
상세 분석
본 논문은 세포 내 물질 운반을 담당하는 키네신‑1 모터가 실제 세포질의 고농도 거대분자와 동적 MAP에 의해 어떻게 조절되는지를 정량적으로 규명하고자 하였다. 실험 설계는 크게 두 축으로 나뉜다. 첫 번째 축은 폴리(ethylene glycol)와 같은 관능성 없는 고분자를 첨가해 용액 내 ‘거대분자 혼탁’(macromolecular crowding) 효과를 재현한 것이다. 이러한 혼탁 환경은 용액 내 유효 부피를 감소시켜 입자 간 ‘배제 효과(depletion interaction)’를 강화한다. 결과적으로 키네신‑1 모터는 미세소관 위에서 평균 이동 거리가 약 1.5배에서 2배로 연장되었으며, 이는 모터가 탈착되지 않고 더 오래 미세소관에 머무르는 시간(association time)이 증가했기 때문이다. 그러나 동시에 비특이적 결합이 증가하여, 모터가 미세소관을 따라 연속적인 전진이 아닌 1‑D 확산 형태로 움직이는 사건이 빈번히 관찰되었다. 이는 고분자 사슬이 미세소관 표면에 얇은 ‘덮개’를 형성해 전기적·입체적 장벽을 완화시키고, 모터와 미세소관 사이의 결합 에너지를 약화시켜 발생하는 현상으로 해석된다.
두 번째 축은 τ(tau)와는 달리 ‘일시적 결합’ 특성을 갖는 MAP, 예를 들어 MAP65와 같은 동적 결합 단백질을 도입한 것이다. 이들 MAP은 미세소관에 짧은 시간 동안만 결합하고 빠르게 해리·재결합을 반복한다. 실험 결과, 일시적 MAP이 존재할 경우 키네신‑1의 평균 전진 속도는 약 20~30 % 감소했지만, 모터의 결합 지속 시간(즉, 탈착 확률)은 크게 변하지 않았다. 이는 일시적 MAP이 물리적 ‘장애물’이라기보다, 미세소관 표면의 ‘점착성’(stickiness)을 순간적으로 변조시켜 모터가 겪는 마찰을 증가시키는 역할을 함을 시사한다. 특히, MAP이 고정된 τ와 달리 지속적인 ‘로드’가 아니므로, 모터가 MAP에 부딪히더라도 우회하거나 일시적으로 정지하는 대신 속도가 감소하는 형태로 전진을 지속한다.
이러한 두 현상의 결합은 세포 내 실제 상황을 더 현실적으로 반영한다. 세포질은 고농도 단백질·핵산·다당류 등으로 구성된 복잡한 매크로분자 네트워크이며, 동시에 다양한 MAP이 동적으로 결합·해리한다. 따라서 키네신 기반 운반은 단순히 ‘고정된 장애물’만을 피하는 것이 아니라, ‘혼탁에 의한 장거리 이동 촉진’과 ‘동적 MAP에 의한 속도 조절’이라는 두 축의 상호작용을 통해 최적화된다.
본 연구는 다음과 같은 핵심 통찰을 제공한다. 첫째, 거대분자 혼탁은 키네신의 ‘프로세시티’(processivity)를 향상시켜 장거리 운반 효율을 높인다. 둘째, 혼탁은 비특이적 결합과 확산을 유발해 운반 정확성을 저해할 가능성이 있다. 셋째, 일시적 MAP은 모터 속도를 조절하지만 결합 지속 시간에는 큰 영향을 주지 않아, 세포는 이러한 MAP을 이용해 운반 속도를 미세하게 튜닝할 수 있다. 넷째, 고정된 τ와 같은 ‘영구적 장애물’과는 달리, 동적 MAP은 운반 경로를 완전히 차단하지 않으면서도 물리적 저항을 제공한다. 이러한 결과는 세포 내 물질 운반 모델링에 새로운 파라미터(혼탁도, MAP 동역학)를 포함시켜야 함을 시사한다.