CRISPR‑dCas9‑mEos3.1 기반 PALM으로 텔로미어 초고해상도 시각화
초록
연구팀은 내핵 효소 활성을 제거한 dCas9에 광전환 형광단백질 mEos3.1을 결합시켜, PALM 기법으로 인간 및 마우스 세포의 텔로미어를 200 nm 이하의 해상도로 관찰하였다. Tet‑Off/On 시스템을 이용해 발현량을 조절하고, sgRNA‑텔로미어 타깃을 통해 특이적 라벨링을 확인하였다. 결과는 정상 마우스 섬유아세포와 ALT‑양성 인간 골육종 세포에서 텔로미어 크기의 차이를 정량화했으며, CRISPR 기반 초고해상도 이미징의 가능성을 제시한다.
상세 분석
본 논문은 기존의 CRISPR‑dCas9‑EGFP 시스템이 회절 제한 해상도에 머물렀던 한계를 극복하기 위해, 광전환 형광단백질인 mEos3.1을 C‑말단에 융합한 dCas9‑mEos3.1 프로브를 설계하였다. mEos3.1은 단일체(monomeric)이며 높은 광자 수와 낮은 다이머화 경향을 갖추고 있어 PALM(Photo‑Activated Localization Microscopy)에서 필수적인 단일분자 신호 대 잡음비를 크게 향상시킨다. 연구진은 dCas9(D10A)와 dCas9(D10A/H840A) 두 가지 불활성 변이를 사용했으며, 각각을 Tet‑Off 및 Tet‑On 조절 시스템에 삽입해 발현량을 정밀하게 제어하였다. 이는 핵 내 자유롭게 확산되는 dCas9‑mEos3.1이 배경 신호를 유발하는 것을 최소화하고, 목표 DNA에 결합된 신호만을 효율적으로 수집하게 한다.
세포주로는 인간 골육종 세포주 U2OS와 마우스 배아 섬유아세포(MEF)를 선택했으며, 두 세포 모두 lentiviral transduction을 통해 안정적인 dCas9‑mEos3.1 및 텔로미어‑특이 sgRNA를 도입하였다. 실험 전 48 h 동안 doxycycline을 제거해 dCas9‑mEos3.1 발현을 유도하고, 고정 전 CSK 버퍼 전처리로 자유 단백질을 제거하였다. 라벨링 특이성은 TRF2(텔로머레픽 반복 결합 단백질 2) 항체와의 공색을 통해 검증했으며, 두 신호가 높은 상관관계를 보임으로써 dCas9‑mEos3.1이 텔로미어에 정확히 결합함을 확인하였다.
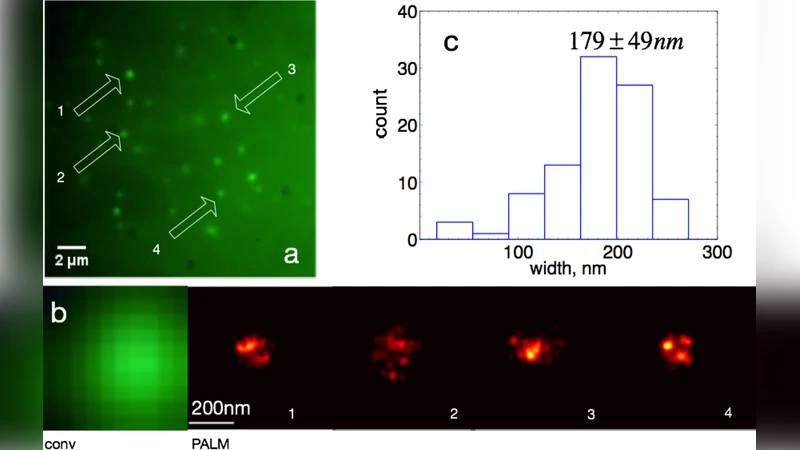
PALM 영상 획득은 405 nm 광으로 mEos3.1을 녹색에서 적색으로 전환하고, 561 nm 레이저로 적색 형광을 연속적으로 촬영하는 방식으로 진행되었다. 초점 고정은 GFP 채널을 이용해 대략적인 위치를 잡은 뒤, 소량의 전환된 신호로 정밀 조정하였다. HILO(Highly Inclined Laminated Optical sheet) 조명을 적용해 배경 플루오레선스를 감소시켰으며, 2,000–6,000 프레임(25 Hz)으로부터 단일분자 위치를 추출해 20–30 nm 수준의 로컬라이제이션 정확도를 달성하였다.
분석 결과, MEF 세포의 텔로미어 평균 직경은 179 ± 49 nm였으며, 이는 기존 PNA‑STORM 연구와 일치한다. 반면 ALT‑양성 U2OS 세포에서는 평균 215 ± 88 nm로 더 넓은 분포와 일부 큰 집합체가 관찰되었다. 이는 ALT 메커니즘이 텔로미어 길이와 구조를 다양하게 변형시킨다는 기존 보고와 부합한다. 또한, dCas9(D10A/H840A) 변이를 사용한 Tet‑On 시스템에서도 유사한 해상도와 크기 측정값을 얻어, 발현 조절 방식에 관계없이 프로브의 성능이 일관됨을 보여준다.
본 연구는 CRISPR‑dCas9 기반 라벨링이 FISH와 달리 DNA 변성을 요구하지 않으며, 살아있는 세포에서도 실시간 초고해상도 이미징이 가능하다는 장점을 강조한다. 다만, 현재는 반복 서열(텔로미어)만을 대상으로 했으며, 단일 복제수 서열에 대한 라벨링 효율, 오프 타깃 결합에 의한 배경, 그리고 광전환 효율에 따른 이미지 품질 변동 등이 향후 과제로 남는다. 저자들은 orthogonal sgRNA를 이용한 다중 색상 dCas9 라벨링, 고특이성 sgRNA 설계, 그리고 더 작은 형광단백질(예: mMaple3) 도입 등을 통해 복합적인 3D 게놈 구조를 정밀히 매핑할 수 있을 것으로 전망한다.
댓글 및 학술 토론
Loading comments...
의견 남기기